De behandeling van sepsis en septische shock moet worden uitgevoerd als een medisch noodgeval (Cecconi et al., 2018). TIJD IS CRUCIAAL! Snelle herkenning, vroege resuscitatie, vroege antibiotica en eliminatie van de bron van infectie zijn dus de belangrijkste componenten voor het leveren van hoogwaardige sepsiszorg. Vroege en optimale hemodynamische resuscitatie is cruciaal. Zowel te weinig als te veel vochtresuscitatie kan leiden tot een ongunstige uitkomst voor de patiënt. Evaluatie van de volumestatus en respons van de patiënt is de hoeksteen voor het beheer van sepsis op de spoedgevallendienst. (Worapratya & Wuthisuthimethawee, 2019) Veel studies hebben aangetoond dat vertraagde resuscitatie het verband houdt met een verhoogde mortaliteit (Coopersmith et al., 2018; Leisman et al., 2018; Morley, 2018). Daarnaast stijgt de mortaliteit bij vertraging in de toediening van de adequate antibiotica (Coopersmith et al., 2018; Hanrath & Hamel, 2017).
Een vroege aanpak en een passende aanpak in de eerste uren na de ontwikkeling van sepsis verbetert de outcome van de patiënt. In de SSC richtlijnen staat dat deze patiënten dringend onderzocht en behandeld moeten worden. Dit omvat eerste vochtresuscitatie, identificatie van de infectiebron, het verkrijgen van de eerste labowaarden en hemodynamische metingen. Een leidend principe is dat deze patiënten behoefte hebben aan een gedetailleerd eerste onderzoek en vervolgens aan een continue herbeoordeling van hun reactie op de behandeling. (Levy et al., 2018)
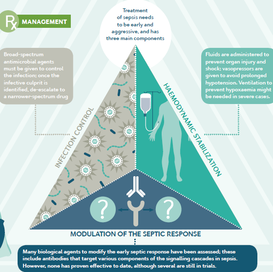
Het beleid is gebaseerd op drie pijlers: infectiebeheersing, hemodynamische stabilisatie + optimalisatie van de oxygenatie en modulatie van de septische respons. (Coopersmith et al., 2018; Hotchkiss et al., 2017) De behandeling op spoed is gericht op het optimaliseren van een vroege herkenning en een snelle eerste benadering van de sepsispatiënt waarbij vermijdbare vertragingen worden geëlimineerd of verminderd. Een correcte klinische aanpak en vroege doelgerichte therapie is de beste aanpak op spoedgevallen. (Charitos et al., 2019)
Een vroege aanpak en een passende aanpak in de eerste uren na de ontwikkeling van sepsis verbetert de outcome van de patiënt. In de SSC richtlijnen staat dat deze patiënten dringend onderzocht en behandeld moeten worden. Dit omvat eerste vochtresuscitatie, identificatie van de infectiebron, het verkrijgen van de eerste labowaarden en hemodynamische metingen. Een leidend principe is dat deze patiënten behoefte hebben aan een gedetailleerd eerste onderzoek en vervolgens aan een continue herbeoordeling van hun reactie op de behandeling. (Levy et al., 2018)
Het beleid is gebaseerd op drie pijlers: infectiebeheersing, hemodynamische stabilisatie + optimalisatie van de oxygenatie en modulatie van de septische respons. (Coopersmith et al., 2018; Hotchkiss et al., 2017) De behandeling op spoed is gericht op het optimaliseren van een vroege herkenning en een snelle eerste benadering van de sepsispatiënt waarbij vermijdbare vertragingen worden geëlimineerd of verminderd. Een correcte klinische aanpak en vroege doelgerichte therapie is de beste aanpak op spoedgevallen. (Charitos et al., 2019)
Infectiebestrijding
De eerste prioriteit bij de behandeling is het starten van adequate antibiotica therapie en het lokaliseren van de oorzaak van de infectie. Dit kan aan de hand van kliniek, beeldvorming, een uitgebreid bloedonderzoek inclusief hemoculturen en afname van andere relevante culturen. De antibioticatherapie moet zo snel mogelijk gestart worden, bij voorkeur nadat de hemoculturen en andere staalnamen gebeurd zijn. Het is niet nodig om te wachten op de resultaten van de laboratoriumonderzoeken. Onderzoek toont aan dat wanneer de antibioticatherapie niet wordt gestart binnen 1 tot 3 uur na aankomst van de patiënt in het ziekenhuis dit gepaard gaat met een hogere mortaliteit. Er wordt aangeraden om te starten met een breedspectrum antibioticum. Van zodra de resultaten van de genomen kweken bekend zijn, zal de antibioticatherapie aangepast worden. Bij sommige kweken zullen verschillende bacteriën geïdentificeerd worden en bij 30% van de genomen culturen zijn de kweken vals negatief en is het niet mogelijk om een gerichte antibioticatherapie te geven. Van zodra de antibioticatherapie gestart is, kan deze gestuurd en geoptimaliseerd worden door het gebruik van biomarkers zoals procalcitonine. Verder is het belangrijk om zo snel mogelijk de infectiehaard onder controle te brengen of te verwijderen. In sommige gevallen zal het ook nodig zijn om de infectie te bestrijden door middel van chirurgie. (Cecconi et al., 2018; Charitos, Topi, Castellaneta, & D'Agostino, 2019; Dieperink, & Pickkers, 2017; Evans, 2018; Hotchkiss et al., 2017; Rhodes et al., 2017; van der Steen,; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
Hemodynamische stabilisatie + optimalisatie van de ventilatie
Het is natuurlijk vanzelfsprekend dat elke patiënt benaderd moet worden volgens het ABCDE-principe. Dit houdt in dat de ademweg, de ademhaling en de circulatie veilig gesteld moeten worden. Indien nodig wordt er dus direct zuurstof toegediend en zo nodig wordt er gestart met kunstmatige ventilatie. (Wiersinga et al., 2017) ‘The Sepsis Six’ beveelt aan om de saturatie boven of gelijk aan 94% te houden. Deze bundel wordt verder besproken onder zorgbundels.
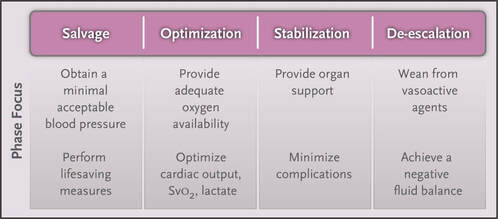
Er zijn vier fasen in de behandeling en therapeutische doelen en monitoring moeten aan elke fase worden aangepast. Deze vier fasen van resuscitatie zijn redding, optimalisatie, stabilisatie en de de-escalatie. (Vincent & De Backer, 2013; Worapratya & Wuthisuthimethawee, 2019) De reddingsfase of levensbedreigende fase wordt gekenmerkt door sterke vasodilatatie en veroorzaakt hypotensie en verminderde orgaanperfusie en vindt plaats binnen enkele minuten tot uren. Vroege en adequate vloeistofresuscitatie wordt toegediend om cardiovasculaire collaps en overlijden te voorkomen. De Sepsis Campaign Guideline 2018 adviseert onmiddellijke toediening van vloeistof in een dosis van 30 ml/kg intraveneuze kristalloïde vloeistof aan bij septische patiënten met een verhoogd lactaatniveau of hypotensie. (Cecconi, Evans, Levy, & Rhodes, 2018; Worapratya & Wuthisuthimethawee, 2019) Het doel in de eerste fase van de therapie is het bereiken van een minimale bloeddruk en cardiale output die compatibel zijn met onmiddellijke overleving. Minimale monitoring is nodig, meestal is dit beperkt tot invasieve monitoring via arteriële katheter en centraal veneuze katheters. Antibiotica wordt toegediend om de onderliggende oorzaak te behandelen. (Vincent & De Backer, 2013)
De optimalisatiefase, die ook reperfusie- en ischemiefase wordt genoemd, vindt binnen enkele uren plaats. In deze periode is een zorgvuldige beoordeling van de intravasculaire volumestatus en het bepalen van de behoefte van verder vocht cruciaal. Zodra adequate intravasculaire volumestatus is bereikt, is het snel toedienen van vasopressortherapie in de setting van vloeistof-refractaire shock een tijdkritische interventie. Wanneer de vasopressortherapie te traag wordt gestart kan dit leiden tot overmatige vochtresuscitatie en verhoogde morbiditeit en mortaliteit. Aanvankelijke vasopressorkeuze bij septische shock is noradrenaline, beginnen bij een dosis van 0,5 mcg/kg/minuut. (Worapratya & Wuthisuthimethawee, 2019) Het doel is om de cellulaire zuurstofbeschikbaarheid te vergroten en interventies die gericht zijn op de hemodynamische status. Metingen van SvO² en lactaat kunnen een hulpmiddel zijn om de therapie te begeleiden. (Vincent & De Backer, 2013)
De stabilisatiefase vindt gewoonlijk plaats binnen een paar dagen en na toediening van geoptimaliseerde vloeistof, wat zich manifesteert door een stabiele hemodynamische toestand. Het doel in deze fase is het behouden van het intravasculair volume, het vervangen van vochtverlies, het ondersteunen van orgaandisfunctie en het voorkomen van iatrogene schade met onnodige intraveneuze vochttoediening. (Worapratya & Wuthisuthimethawee, 2019) Het doel is het voorkomen van orgaandisfunctie, ook nadat de hemodynamische stabiliteit is bereikt. De zuurstoftoevoer naar de weefsels is niet langer het belangrijkste probleem en de ondersteuning van de organen wordt relevanter. (Vincent & De Backer, 2013)
De de-escalatiefase wordt gekenmerkt door orgaanherstel, het weanen van de kunstmatige ventilatie en vasopressorondersteuning. In deze fase wordt getracht een algehele negatieve vochtbalans te bereiken. Er is aangetoond dat er een onafhankelijk verband bestaat tussen een verhoogde positieve vochtbalans en een verhoogde mortaliteit. Het toedienen van diuretica dient voorzichtig te gebeuren zonder het induceren van hypotensie en het verminderen van de cardiale output. (Vincent & De Backer, 2013; Worapratya & Wuthisuthimethawee, 2019)
De eerste prioriteit bij de behandeling is het starten van adequate antibiotica therapie en het lokaliseren van de oorzaak van de infectie. Dit kan aan de hand van kliniek, beeldvorming, een uitgebreid bloedonderzoek inclusief hemoculturen en afname van andere relevante culturen. De antibioticatherapie moet zo snel mogelijk gestart worden, bij voorkeur nadat de hemoculturen en andere staalnamen gebeurd zijn. Het is niet nodig om te wachten op de resultaten van de laboratoriumonderzoeken. Onderzoek toont aan dat wanneer de antibioticatherapie niet wordt gestart binnen 1 tot 3 uur na aankomst van de patiënt in het ziekenhuis dit gepaard gaat met een hogere mortaliteit. Er wordt aangeraden om te starten met een breedspectrum antibioticum. Van zodra de resultaten van de genomen kweken bekend zijn, zal de antibioticatherapie aangepast worden. Bij sommige kweken zullen verschillende bacteriën geïdentificeerd worden en bij 30% van de genomen culturen zijn de kweken vals negatief en is het niet mogelijk om een gerichte antibioticatherapie te geven. Van zodra de antibioticatherapie gestart is, kan deze gestuurd en geoptimaliseerd worden door het gebruik van biomarkers zoals procalcitonine. Verder is het belangrijk om zo snel mogelijk de infectiehaard onder controle te brengen of te verwijderen. In sommige gevallen zal het ook nodig zijn om de infectie te bestrijden door middel van chirurgie. (Cecconi et al., 2018; Charitos, Topi, Castellaneta, & D'Agostino, 2019; Dieperink, & Pickkers, 2017; Evans, 2018; Hotchkiss et al., 2017; Rhodes et al., 2017; van der Steen,; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
Hemodynamische stabilisatie + optimalisatie van de ventilatie
Het is natuurlijk vanzelfsprekend dat elke patiënt benaderd moet worden volgens het ABCDE-principe. Dit houdt in dat de ademweg, de ademhaling en de circulatie veilig gesteld moeten worden. Indien nodig wordt er dus direct zuurstof toegediend en zo nodig wordt er gestart met kunstmatige ventilatie. (Wiersinga et al., 2017) ‘The Sepsis Six’ beveelt aan om de saturatie boven of gelijk aan 94% te houden. Deze bundel wordt verder besproken onder zorgbundels.
Er zijn vier fasen in de behandeling en therapeutische doelen en monitoring moeten aan elke fase worden aangepast. Deze vier fasen van resuscitatie zijn redding, optimalisatie, stabilisatie en de de-escalatie. (Vincent & De Backer, 2013; Worapratya & Wuthisuthimethawee, 2019) De reddingsfase of levensbedreigende fase wordt gekenmerkt door sterke vasodilatatie en veroorzaakt hypotensie en verminderde orgaanperfusie en vindt plaats binnen enkele minuten tot uren. Vroege en adequate vloeistofresuscitatie wordt toegediend om cardiovasculaire collaps en overlijden te voorkomen. De Sepsis Campaign Guideline 2018 adviseert onmiddellijke toediening van vloeistof in een dosis van 30 ml/kg intraveneuze kristalloïde vloeistof aan bij septische patiënten met een verhoogd lactaatniveau of hypotensie. (Cecconi, Evans, Levy, & Rhodes, 2018; Worapratya & Wuthisuthimethawee, 2019) Het doel in de eerste fase van de therapie is het bereiken van een minimale bloeddruk en cardiale output die compatibel zijn met onmiddellijke overleving. Minimale monitoring is nodig, meestal is dit beperkt tot invasieve monitoring via arteriële katheter en centraal veneuze katheters. Antibiotica wordt toegediend om de onderliggende oorzaak te behandelen. (Vincent & De Backer, 2013)
De optimalisatiefase, die ook reperfusie- en ischemiefase wordt genoemd, vindt binnen enkele uren plaats. In deze periode is een zorgvuldige beoordeling van de intravasculaire volumestatus en het bepalen van de behoefte van verder vocht cruciaal. Zodra adequate intravasculaire volumestatus is bereikt, is het snel toedienen van vasopressortherapie in de setting van vloeistof-refractaire shock een tijdkritische interventie. Wanneer de vasopressortherapie te traag wordt gestart kan dit leiden tot overmatige vochtresuscitatie en verhoogde morbiditeit en mortaliteit. Aanvankelijke vasopressorkeuze bij septische shock is noradrenaline, beginnen bij een dosis van 0,5 mcg/kg/minuut. (Worapratya & Wuthisuthimethawee, 2019) Het doel is om de cellulaire zuurstofbeschikbaarheid te vergroten en interventies die gericht zijn op de hemodynamische status. Metingen van SvO² en lactaat kunnen een hulpmiddel zijn om de therapie te begeleiden. (Vincent & De Backer, 2013)
De stabilisatiefase vindt gewoonlijk plaats binnen een paar dagen en na toediening van geoptimaliseerde vloeistof, wat zich manifesteert door een stabiele hemodynamische toestand. Het doel in deze fase is het behouden van het intravasculair volume, het vervangen van vochtverlies, het ondersteunen van orgaandisfunctie en het voorkomen van iatrogene schade met onnodige intraveneuze vochttoediening. (Worapratya & Wuthisuthimethawee, 2019) Het doel is het voorkomen van orgaandisfunctie, ook nadat de hemodynamische stabiliteit is bereikt. De zuurstoftoevoer naar de weefsels is niet langer het belangrijkste probleem en de ondersteuning van de organen wordt relevanter. (Vincent & De Backer, 2013)
De de-escalatiefase wordt gekenmerkt door orgaanherstel, het weanen van de kunstmatige ventilatie en vasopressorondersteuning. In deze fase wordt getracht een algehele negatieve vochtbalans te bereiken. Er is aangetoond dat er een onafhankelijk verband bestaat tussen een verhoogde positieve vochtbalans en een verhoogde mortaliteit. Het toedienen van diuretica dient voorzichtig te gebeuren zonder het induceren van hypotensie en het verminderen van de cardiale output. (Vincent & De Backer, 2013; Worapratya & Wuthisuthimethawee, 2019)

Vochtresuscitatie is de eerste interventie bij een sepsis patiënt met hypotensie (van der Steen, Dieperink, & Pickkers, 2017). Vroegtijdige effectieve vloeistofresuscitatie is cruciaal voor stabilisatie van sepsis-geïnduceerde weefselhypoperfusie of septische shock. Sepsis-geïnduceerde hypoperfusie kan zich manifesteren door acute orgaandisfunctie en/of hypotensie en verhoogde serumlactaat (Rhodes et al., 2017). Oorspronkelijk werd de voorkeur gegeven aan colloïdale vloeistoffen, deze zorgen namelijk voor een betere intravasale volume-expansie. Uit onderzoek blijkt echter dat deze patiënten die deze therapie hadden gekregen een grotere mortaliteit hadden en dat zij vaker nood hadden aan dialyse. Nu wordt de voorkeur gegeven aan kristalloïde vloeistoffen. (Alhazzani et al., 2020; Coopersmith et al., 2018; Levy et al., 2018;; Cecconi et al., 2018; Rhodes et al., 2017; van der Steen et al., 2017) Het gebruik van kristalloïde boven colloïden wordt aanbevolen omwille van het feit dat colloïden schadelijk zijn, ook zijn colloïden duurder dan kristalloïde en is de beschikbaarheid van colloïden in sommige landen beperkt (bijvoorbeeld in sommige landen met een laag of gemiddeld inkomen). (Alhazzani et al., 2020) Ook hebben meerdere studies vochtresuscitatie vergeleken op basis van kristalloïden en colloïden, zonder duidelijk voordeel voor colloïden. Dus gezien de verhoogde kosten in verband met colloïde vloeistoffen en het verhoogde risico op nefrotoxiciteit (behalve bij albumine), worden kristalloïde vloeistoffen geadviseerd. (Cecconi et al., 2018)
De fundamentele redenering voor het toedienen van vocht is het verbeteren van de weefselperfusie door het vergroten van de cardiale output (Coopersmith et al., 2018). De belangrijkste vraag is echter of er effectief vloeistof moet gegeven worden en hoeveel vloeistof er al dan niet gegeven moet worden (Coopersmith et al., 2018; van der Steen et al., 2017). De SSC adviseert een snelle toediening van 30ml/kg kristalloïde vloeistof voor hypotensie of lactaat > 4 mmol/L. (Cecconi et al., 2018; Coopersmith et al., 2018). Na de eerste vochtresuscitatie zal het toedienen van aanvullende vloeistoffen geleid worden door een frequente beoordeling van de hemodynamische toestand. De herbeoordeling dient een grondig klinisch onderzoek en evaluatie van de beschikbare fysiologische variabelen (hartslag, bloeddruk, arteriële zuurstofverzadiging, ademhalingssnelheid, temperatuur, urineafgifte en andere) te omvatten, evenals andere niet-invasieve of invasieve monitoring, voor zover beschikbaar. (Rhodes et al., 2017)
De methoden voor het bepalen van de vloeistofresponsiviteit omvatten de toepassing van empirische vloeistofbolussen, statische metingen en dynamische markers. De empirische toediening van een vochtbolus is problematisch. Dit omdat een aantal patiënten niet zullen reageren, wat schadelijk kan zijn. Het ergste scenario is wanneer deze empirische toediening wordt gedaan zonder enige meting van de effectiviteit en de tolerantie, wat vaak kan leiden tot herhaalde toedieningen wanneer het probleem dat dat de toediening van de vloeistof in gang zet, aanhoudt. (Coopersmith et al., 2018) SSC adviseert dynamische parameters, temperatuur, capillaire refill en/of serumlactaat boven statistische parameters te gebruiken om de vloeistofresponsiviteit te beoordelen (Alhazzani et al., 2020; Rhodes et al., 2017). Dynamische maatregelen omvatten een verscheidenheid aan technologieën om de verandering in de cardiale output te beoordelen als reactie op voorbijgaande veranderingen in de voorbelasting geïnduceerd door beademing of een extern manoeuvre, voorafgaand aan de toediening van de vloeistof (Coopersmith et al., 2018). Deze technieken omvatten variatie in slagvolume (SVV), variatie in polsdruk (PPV) en verandering in slagvolume bij passieve verhoging van de benen (Alhazzani et al., 2020; Coopersmith et al., 2018; Rhodes et al., 2017). Onder de onderzochte dynamische parameters lijkt passieve beenverhoging, gevolgd door PPV en SVV de vloeistofresponsiviteit met de hoogste nauwkeurigheid te voorspellen (Alhazzani et al., 2020; Rhodes et al., 2017). Variaties in ademhalingspatronen, of polsdruk en slagvolume kunnen echter moeilijk te interpreteren zijn bij spontaan ademende patiënten (Coopersmith et al., 2018).
Door het gebruik van, zoals eerder vermeld, dynamische parameters en niet-invasieve bepalingen van het hartminuutvolume zoals echografie, kan er nagegaan worden of de vochtbolus een verhoging van de cardiac output heeft veroorzaakt en dus het gewenste effect heeft (van der Steen et al., 2017). Bedside echografie lijkt de beste parameter om vochtresuscitatie op de spoedgevallendienst te begeleiden met een hoge gevoeligheid en specificiteit (Worapratya & Wuthisuthimethawee, 2019). Echografie is de laatste jaren voor veel bedside clinici beschikbaar geworden en maakt een meer gedetaileerde beoordeling van de oorzaken van hemodynamische problemen mogelijk (Rhodes et al., 2017).
Er zijn ook nog andere methodes die kunnen helpen om de vochttoediening te sturen. Eén van deze methodes is de lactaat-gestuurde therapie (Rudd et al., 2018; Specialisten, 2020; Worapratya & Wuthisuthimethawee, 2019). Door het lactaatgehalte op te volgen kan de effectiviteit van de vochtresuscitatie worden opgevolgd (Cecconi et al., 2018; Hotchkiss et al., 2017). Serumlactaat is geen directe maat voor weefselperfusie maar verhoging van het lactaat kan wel duiden op weefselhypoxie, versnelde aërobe glycolyse als gevolg van een overmatige bèta-agressieve stimulatie of andere oorzaken (bijvoorbeeld leverfalen). Ongeacht de bron worden verhoogde lactaatniveaus geassocieerd met een slechtere outcome. Omdat lactaat een standaard laboratoriumtest is met een voorgeschreven technieken voor de meting ervan, kan het dienen als een objectiever surrogaat voor weefselperfusie in vergelijking met lichamelijk onderzoek of urineproductie. In een studie met lactaat-geleide vochtresuscitatie werd een verminderde mortaliteit waargenomen in vergelijking met een resuscitatie zonder lactaat-monitoring. SSC adviseert om resuscitatie op te volgen aan de hand van het lactaatgehalte (Cecconi et al., 2018; Rhodes et al., 2017). Het is een parameter die gemakkelijk en weinig invasief te meten is. De Federatie Medische Specialisten raadt aan om het volgen van het lactaat te gebruiken in combinatie met andere parameters zoals de bloeddruk of MAP. (Specialisten, 2020) Hercontrole van het lactaat wordt door SSC aangeraden binnen twee tot vier uren na initiële lactaatcontrole (Levy et al., 2018).
MAP is de stuwende druk van de weefselperfusie. Terwijl perfusie van kritieke organen zoals de nieren of de hersenen kan worden beschermd door autoregulering van regionale perfusie tegen hypotensie onder een drempelwaarde MAP, wordt weefsel perfusie lineair afhankelijk van de arteriële druk. (Levy et al., 2018) Er dient gestreefd te worden naar een MAP van 65 mmHg (Alhazzani et al., 2020; Hotchkiss et al., 2017; Levy et al., 2018). Hogere MAP waarde geven een verhoogd risico op hartritmestoornissen. Er werd ook verminderde mortaliteit ten gunste van een MAP-doelstelling van 65 mmHg in vergelijking met een standaard MAP-doelstelling. Er wordt geadviseerd om noradrenaline als eerste keuze vasoactief middel te gebruiken om een MAP van 65 mmHg te handhaven (Evans, 2018). (Alhazzani et al., 2020; Rhodes et al., 2017) Noradrenaline is de meest bestudeerde vasoactieve stof met een laag risico op ongewenste effecten en een lagere mortaliteit. (Alhazzani et al., 2020; Hotchkiss et al., 2017) Een mogelijke bijwerking van dopamine is dat het hartritmestoornissen kan veroorzaken. Om de cardiale output en weefselperfusie te verhogen wordt dobutamine vaak toegevoegd aan noradrenaline. (Hotchkiss et al., 2017) Het is echter wel zo dat hoe meer middelen er gebruikt moeten worden om de bloeddruk te verhogen, zoals vocht en/of vasopressie, hoe meer kans de patiënt heeft om complicaties van deze behandelingen op te lopen. Er moet dus gestreefd worden om zoveel vocht te geven als nodig is, maar niet meer dan dat. (Specialisten, 2020)
De vroegtijdige doelgerichte therapie (EGDT) werd in 2001 geïntroduceerd en is een steeds meer omstreden manier om sepsis te behandelen. Deze therapie zou de mortaliteit van sepsispatiënten verminderen. Het is gebaseerd op het bereiken van een centrale veneuze zuurstofverzadiging (SvO²) van meer dan 70% met behulp van intraveneuze vloeistoffen, dobutamine en een eventuele bloedtransfusie om zo een hemodynamische resuscitatie te bereiken. Deze methode werd besproken door Rivers et al. in 2001 maar kon niet worden bevestigd in meer recente, grotere studies (Hotchkiss et al., 2017; Rhodes et al., 2017). Uit analyse blijkt dat EGDT geen betere outcome geeft in vergelijking met de standaardzorg. Het gaat echter wel gepaard met hogere ziekenhuiskosten. Het gebruik van EGDT wordt om deze reden niet meer standaard aangeraden, evenmin als monitoring van de respons op therapie met CVD- en Scvo2-meting. (Rhodes et al., 2017; van der Steen et al., 2017) De centraal veneuze druk is geen goede indicator om vochtresuscitatie te evalueren (Coopersmith et al., 2018; Rhodes et al., 2017; Worapratya & Wuthisuthimethawee, 2019).
Andere observaties die een beeld geven over de weefselperfusie zoals urine-output, mottling score en capillaire refill kunnen gebruikt worden om de vochtresuscitatie op te volgen (Salomao et al., 2019). Eén van de belangrijkste principes om te begrijpen in het beheer van deze complexe patiënten is de noodzaak voor een gedetailleerde eerste beoordeling en een voortdurende herevaluatie van de respons van de behandeling. Deze evaluatie dient te beginnen met een grondig klinisch onderzoek en een evaluatie van de beschikbare fysiologische variabelen die de klinische toestand van de patiënt kunnen beschrijven (hartslag, bloeddruk, arteriële zuurstofsaturatie, ademhalingssnelheid, temperatuur, urine-output en andere beschikbare variabelen). (Rhodes et al., 2017)
Voor de mechanische ventilatie van patiënten met sepsis wordt geadviseerd door het SSC om een laag tidal volume van 6ml/kg te gebruiken in vergelijking met 12ml/kg bij volwassen patiënten met sepsis-geïnduceerde ARDS (Rhodes et al., 2017; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017). Er wordt geadviseerd om te richten op plateau-drukken van < 30cm H2O. Er wordt hoge PEEP geadviseerd boven lage PEEP. (Rhodes et al., 2017) Omdat dit meer behoort tot een onderdeel specifiek voor intensieve zorgen wordt dit niet verder besproken.
Modulatie van de septische respons
Momenteel wordt er nog steeds veel onderzoek gedaan naar vroege klinische interventie met behulp van ontstekingsremmende en immunostimulerende middelen bij sepsis. Er is echter nog steeds verder onderzoek nodig (Cecconi et al., 2018; Hotchkiss et al., 2017).
De fundamentele redenering voor het toedienen van vocht is het verbeteren van de weefselperfusie door het vergroten van de cardiale output (Coopersmith et al., 2018). De belangrijkste vraag is echter of er effectief vloeistof moet gegeven worden en hoeveel vloeistof er al dan niet gegeven moet worden (Coopersmith et al., 2018; van der Steen et al., 2017). De SSC adviseert een snelle toediening van 30ml/kg kristalloïde vloeistof voor hypotensie of lactaat > 4 mmol/L. (Cecconi et al., 2018; Coopersmith et al., 2018). Na de eerste vochtresuscitatie zal het toedienen van aanvullende vloeistoffen geleid worden door een frequente beoordeling van de hemodynamische toestand. De herbeoordeling dient een grondig klinisch onderzoek en evaluatie van de beschikbare fysiologische variabelen (hartslag, bloeddruk, arteriële zuurstofverzadiging, ademhalingssnelheid, temperatuur, urineafgifte en andere) te omvatten, evenals andere niet-invasieve of invasieve monitoring, voor zover beschikbaar. (Rhodes et al., 2017)
De methoden voor het bepalen van de vloeistofresponsiviteit omvatten de toepassing van empirische vloeistofbolussen, statische metingen en dynamische markers. De empirische toediening van een vochtbolus is problematisch. Dit omdat een aantal patiënten niet zullen reageren, wat schadelijk kan zijn. Het ergste scenario is wanneer deze empirische toediening wordt gedaan zonder enige meting van de effectiviteit en de tolerantie, wat vaak kan leiden tot herhaalde toedieningen wanneer het probleem dat dat de toediening van de vloeistof in gang zet, aanhoudt. (Coopersmith et al., 2018) SSC adviseert dynamische parameters, temperatuur, capillaire refill en/of serumlactaat boven statistische parameters te gebruiken om de vloeistofresponsiviteit te beoordelen (Alhazzani et al., 2020; Rhodes et al., 2017). Dynamische maatregelen omvatten een verscheidenheid aan technologieën om de verandering in de cardiale output te beoordelen als reactie op voorbijgaande veranderingen in de voorbelasting geïnduceerd door beademing of een extern manoeuvre, voorafgaand aan de toediening van de vloeistof (Coopersmith et al., 2018). Deze technieken omvatten variatie in slagvolume (SVV), variatie in polsdruk (PPV) en verandering in slagvolume bij passieve verhoging van de benen (Alhazzani et al., 2020; Coopersmith et al., 2018; Rhodes et al., 2017). Onder de onderzochte dynamische parameters lijkt passieve beenverhoging, gevolgd door PPV en SVV de vloeistofresponsiviteit met de hoogste nauwkeurigheid te voorspellen (Alhazzani et al., 2020; Rhodes et al., 2017). Variaties in ademhalingspatronen, of polsdruk en slagvolume kunnen echter moeilijk te interpreteren zijn bij spontaan ademende patiënten (Coopersmith et al., 2018).
Door het gebruik van, zoals eerder vermeld, dynamische parameters en niet-invasieve bepalingen van het hartminuutvolume zoals echografie, kan er nagegaan worden of de vochtbolus een verhoging van de cardiac output heeft veroorzaakt en dus het gewenste effect heeft (van der Steen et al., 2017). Bedside echografie lijkt de beste parameter om vochtresuscitatie op de spoedgevallendienst te begeleiden met een hoge gevoeligheid en specificiteit (Worapratya & Wuthisuthimethawee, 2019). Echografie is de laatste jaren voor veel bedside clinici beschikbaar geworden en maakt een meer gedetaileerde beoordeling van de oorzaken van hemodynamische problemen mogelijk (Rhodes et al., 2017).
Er zijn ook nog andere methodes die kunnen helpen om de vochttoediening te sturen. Eén van deze methodes is de lactaat-gestuurde therapie (Rudd et al., 2018; Specialisten, 2020; Worapratya & Wuthisuthimethawee, 2019). Door het lactaatgehalte op te volgen kan de effectiviteit van de vochtresuscitatie worden opgevolgd (Cecconi et al., 2018; Hotchkiss et al., 2017). Serumlactaat is geen directe maat voor weefselperfusie maar verhoging van het lactaat kan wel duiden op weefselhypoxie, versnelde aërobe glycolyse als gevolg van een overmatige bèta-agressieve stimulatie of andere oorzaken (bijvoorbeeld leverfalen). Ongeacht de bron worden verhoogde lactaatniveaus geassocieerd met een slechtere outcome. Omdat lactaat een standaard laboratoriumtest is met een voorgeschreven technieken voor de meting ervan, kan het dienen als een objectiever surrogaat voor weefselperfusie in vergelijking met lichamelijk onderzoek of urineproductie. In een studie met lactaat-geleide vochtresuscitatie werd een verminderde mortaliteit waargenomen in vergelijking met een resuscitatie zonder lactaat-monitoring. SSC adviseert om resuscitatie op te volgen aan de hand van het lactaatgehalte (Cecconi et al., 2018; Rhodes et al., 2017). Het is een parameter die gemakkelijk en weinig invasief te meten is. De Federatie Medische Specialisten raadt aan om het volgen van het lactaat te gebruiken in combinatie met andere parameters zoals de bloeddruk of MAP. (Specialisten, 2020) Hercontrole van het lactaat wordt door SSC aangeraden binnen twee tot vier uren na initiële lactaatcontrole (Levy et al., 2018).
MAP is de stuwende druk van de weefselperfusie. Terwijl perfusie van kritieke organen zoals de nieren of de hersenen kan worden beschermd door autoregulering van regionale perfusie tegen hypotensie onder een drempelwaarde MAP, wordt weefsel perfusie lineair afhankelijk van de arteriële druk. (Levy et al., 2018) Er dient gestreefd te worden naar een MAP van 65 mmHg (Alhazzani et al., 2020; Hotchkiss et al., 2017; Levy et al., 2018). Hogere MAP waarde geven een verhoogd risico op hartritmestoornissen. Er werd ook verminderde mortaliteit ten gunste van een MAP-doelstelling van 65 mmHg in vergelijking met een standaard MAP-doelstelling. Er wordt geadviseerd om noradrenaline als eerste keuze vasoactief middel te gebruiken om een MAP van 65 mmHg te handhaven (Evans, 2018). (Alhazzani et al., 2020; Rhodes et al., 2017) Noradrenaline is de meest bestudeerde vasoactieve stof met een laag risico op ongewenste effecten en een lagere mortaliteit. (Alhazzani et al., 2020; Hotchkiss et al., 2017) Een mogelijke bijwerking van dopamine is dat het hartritmestoornissen kan veroorzaken. Om de cardiale output en weefselperfusie te verhogen wordt dobutamine vaak toegevoegd aan noradrenaline. (Hotchkiss et al., 2017) Het is echter wel zo dat hoe meer middelen er gebruikt moeten worden om de bloeddruk te verhogen, zoals vocht en/of vasopressie, hoe meer kans de patiënt heeft om complicaties van deze behandelingen op te lopen. Er moet dus gestreefd worden om zoveel vocht te geven als nodig is, maar niet meer dan dat. (Specialisten, 2020)
De vroegtijdige doelgerichte therapie (EGDT) werd in 2001 geïntroduceerd en is een steeds meer omstreden manier om sepsis te behandelen. Deze therapie zou de mortaliteit van sepsispatiënten verminderen. Het is gebaseerd op het bereiken van een centrale veneuze zuurstofverzadiging (SvO²) van meer dan 70% met behulp van intraveneuze vloeistoffen, dobutamine en een eventuele bloedtransfusie om zo een hemodynamische resuscitatie te bereiken. Deze methode werd besproken door Rivers et al. in 2001 maar kon niet worden bevestigd in meer recente, grotere studies (Hotchkiss et al., 2017; Rhodes et al., 2017). Uit analyse blijkt dat EGDT geen betere outcome geeft in vergelijking met de standaardzorg. Het gaat echter wel gepaard met hogere ziekenhuiskosten. Het gebruik van EGDT wordt om deze reden niet meer standaard aangeraden, evenmin als monitoring van de respons op therapie met CVD- en Scvo2-meting. (Rhodes et al., 2017; van der Steen et al., 2017) De centraal veneuze druk is geen goede indicator om vochtresuscitatie te evalueren (Coopersmith et al., 2018; Rhodes et al., 2017; Worapratya & Wuthisuthimethawee, 2019).
Andere observaties die een beeld geven over de weefselperfusie zoals urine-output, mottling score en capillaire refill kunnen gebruikt worden om de vochtresuscitatie op te volgen (Salomao et al., 2019). Eén van de belangrijkste principes om te begrijpen in het beheer van deze complexe patiënten is de noodzaak voor een gedetailleerde eerste beoordeling en een voortdurende herevaluatie van de respons van de behandeling. Deze evaluatie dient te beginnen met een grondig klinisch onderzoek en een evaluatie van de beschikbare fysiologische variabelen die de klinische toestand van de patiënt kunnen beschrijven (hartslag, bloeddruk, arteriële zuurstofsaturatie, ademhalingssnelheid, temperatuur, urine-output en andere beschikbare variabelen). (Rhodes et al., 2017)
Voor de mechanische ventilatie van patiënten met sepsis wordt geadviseerd door het SSC om een laag tidal volume van 6ml/kg te gebruiken in vergelijking met 12ml/kg bij volwassen patiënten met sepsis-geïnduceerde ARDS (Rhodes et al., 2017; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017). Er wordt geadviseerd om te richten op plateau-drukken van < 30cm H2O. Er wordt hoge PEEP geadviseerd boven lage PEEP. (Rhodes et al., 2017) Omdat dit meer behoort tot een onderdeel specifiek voor intensieve zorgen wordt dit niet verder besproken.
Modulatie van de septische respons
Momenteel wordt er nog steeds veel onderzoek gedaan naar vroege klinische interventie met behulp van ontstekingsremmende en immunostimulerende middelen bij sepsis. Er is echter nog steeds verder onderzoek nodig (Cecconi et al., 2018; Hotchkiss et al., 2017).
Zorgbundels
Implementatie van een richtlijn voor het beleid bij patiënten met sepsis, de sepsisbundel, waarin eenvoudige evidence based aanbevelingen worden gedaan, heeft geleid tot het verlagen van de mortaliteit. Het snel herkennen van sepsis, snelle en adequate vloeistofresuscitatie, het toedienen van antibiotica en het onder controle krijgen van de infectiehaard zijn hierbij de belangrijkste uitgangspunten. (Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017) Er zijn verschillende zorgbundels gemaakt om dergelijke zorg te stroomlijnen. Het is een nuttige manier om ervoor te zorgen dat belangrijke stappen in het beheer niet worden vergeten. De meest actuele richtlijnen zijn die van de Surviving Sepsis Campaign. (Evans, 2018) De SSC, die tot doel heeft de sterfte aan sepsis te verminderen door snelle diagnostiek en adequate behandeling, is instrumenteel geweest in de succesvolle wereldwijde implementatie van behandelrichtlijnen voor sepsis. (Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017) The sepsis six en de bundels van de Surviving Sepsis Campaign worden verder besproken.
The sepsis six
‘The Sepsis Six’ is de naam voor een bundel van handelingen die gebruikt worden om de mortaliteit bij sepsis te verminderen (Day, 2020). De bundel is ontwikkeld in het Verenigd Koninkrijk en is goedgekeurd door de Sepsis Trust. Het is een nuttige manier om ervoor te zorgen dat belangrijke stappen in het beheer niet worden vergeten en wordt veel gebruikt in Britse ziekenhuizen. (Evans, 2018) Bijkomend vergemakkelijkt het ook de te nemen interventies(Kumar, Jordan, Caesar, & Miller, 2015). Volgens een onderzoek van Kumar et al. (2015) heeft het toepassen van de Sepsis Six een risicovermindering op overlijden van 55%, dit heeft zich echter niet vertaald in betere patiënten resultaten op gebied van mortaliteit.
De Sepsis Six bestaat uit drie diagnostische en monitoring stappen en drie therapeutische interventies (Kumar et al., 2015).
De UK Sepsis Trust heeft screening- en actie-instrumenten geproduceerd die de aanbevelingen in de NICE-richtlijn over sepsis nauwkeurig weergeven en ondersteunen de NICE-kwaliteitsnorm voor sepsis. (NICE, 2019)
NICE, het National Institute for Health and Care Excellence, biedt nationale begeleiding en advies in het Verenigd Koninkrijk om gezondheids- en sociale zorg te verbeteren. Hoewel sepsis multifactorieel is en zelden op delfde manier voorkomt was de Guideline Development Group, die richtlijnen maken, van mening dat het gebruik van een eenvoudige, gestructureerde risicobeoordeling clinici kan helpen bij het identificeren van de ernstige ziekten die onmiddellijk een potentieel levensreddende behandeling nodig hebben. Deze richtlijn zorgt ervoor dat patiënten die volgens recente definities als sepsis worden gedefinieerd, minimaal worden beoordeeld als een matig hoog risico. Deze leidraad gaat ook over passende deëscalatie als sepsis onwaarschijnlijk is en breedspectrumantibiotica of ziekenhuisopname niet geschikt zijn. NICE heeft een richtlijn voor de herkenning, diagnose en behandelingen van sepsis bij kinderen en volwassenen. De aanbevelingen zijn gebaseerd op een systematische evaluatie van het beste beschikbare bewijsmateriaal en een expliciete overweging van de kosteneffectiviteit. Wanneer er minimaal bewijs beschikbaar is, zijn de aanbevelingen gebaseerd op de ervaring van de Guideline Development Group en de mening over wat een goede praktijk is. Mensen met sepsis kunnen niet specifieke, niet-lokale presentatie hebben, zoals een zeer ziek gevoel hebben en hoeven niet noodzakelijk koorts te hebben. Besteed bijzondere aandacht aan de zorgen die de patiënt en de familie of verzorgers uiten, zoals een verandering van het gebruikelijk gedrag. Wees extra voorzichtig als mensen geen goede geschiedenis kunnen geven, zoals mensen met een andere taal of met communicatieproblemen. Beoordeel mensen met een vermoedelijke infectie en identificeer:
Als een persoon een infectie heeft en er is klinische bezorgdheid voor mogelijke sepsis, voer dan een gestructureerde beoordeling uit met behulp van de voorgeschiedenis en lichamelijk onderzoek om het risico op ernstige ziekte of overlijden door sepsis te beoordelen. Wees alert op veranderingen in gedrag, in het bijzonder een nieuwe verandering van mentale toestand, zijn een sterke risicofactor voor sterfte. Tachypnoe wordt geassocieerd met een slecht resultaat voor de patiënt en een slechte diagnose van de infectie, vooral omdat pneumonie een veelvoorkomende oorzaak is van sepsis. Extreme waarden van bloeddruk zijn een reden tot klinische bezorgdheid. Bloeddruk moet echter geïnterpreteerd worden in de context van de eerdere bloeddruk van een persoon als deze bekend is. Tachycardie is een risicofactor voor ernstige infecties, sepsis, voor opname op de intensieve zorgenafdeling en voor sterfte. Koorts kan een risicofactor zijn voor sepsis, hoewel sommige studies aantoonden dat een groot deel van de patiënten met sepsis geen verhoogde temperatuur had, dit met name oudere mensen, mensen die een kankerbehandeling krijgen en degene die ernstig ziek zijn met sepsis hebben minder kans om een verhoogde temperatuur te ontwikkelen. Een gemarmerd uiterlijk en cyanose van de huid, de lippen of de tong zijn markers met een hoog risico op ernstige ziekte of overlijden. (Freitag et al., 2016)
Personen die zijn geclassificeerd als personen met een hoog risico op sepsis hebben antibiotica en vloeistoffen nodig en mogelijk ondersteunende zorg. De behandeling moet tijdig worden uitgevoerd en kan gespecialiseerde en kritische zorg vereisen. Gebruik point of care lactaat testen om de vloeistoftherapie en mogelijke betrokkenheid van kritische zorg te begeleiden. Als onderdeel van de eerste beoordeling moet worden gezocht naar een infectiebron, inclusief bronnen die mogelijk een chirurgische drainage nodig hebben. Doelwit testen volgens geschiedenis en onderzoek bijvoorbeeld een urineanalyse voor mensen met een vermoeden van een urineweg sepsis. Beeldvorming van de buik en bekken moet worden overwogen als er geen waarschijnlijke bron wordt geïdentificeerd na klinisch onderzoek en eerste tests. NICE aanbevelingen adviseren om zeker aandacht te schenken aan ‘think sepsis!”, aan sepsis te denken bij elke persoon met een vermoedelijke infectie. (Freitag et al., 2016) De NICE sepsis guidance is hieronder terug te vinden.
The sepsis six
‘The Sepsis Six’ is de naam voor een bundel van handelingen die gebruikt worden om de mortaliteit bij sepsis te verminderen (Day, 2020). De bundel is ontwikkeld in het Verenigd Koninkrijk en is goedgekeurd door de Sepsis Trust. Het is een nuttige manier om ervoor te zorgen dat belangrijke stappen in het beheer niet worden vergeten en wordt veel gebruikt in Britse ziekenhuizen. (Evans, 2018) Bijkomend vergemakkelijkt het ook de te nemen interventies(Kumar, Jordan, Caesar, & Miller, 2015). Volgens een onderzoek van Kumar et al. (2015) heeft het toepassen van de Sepsis Six een risicovermindering op overlijden van 55%, dit heeft zich echter niet vertaald in betere patiënten resultaten op gebied van mortaliteit.
De Sepsis Six bestaat uit drie diagnostische en monitoring stappen en drie therapeutische interventies (Kumar et al., 2015).
- Geef zuurstof zodat saturatie > 94%
- Neem hemoculturen
- Geef antibiotica
- Start vochtresuscitatie
- Controleer lactaatgehalte
- Monitor elk uur de urine-output
De UK Sepsis Trust heeft screening- en actie-instrumenten geproduceerd die de aanbevelingen in de NICE-richtlijn over sepsis nauwkeurig weergeven en ondersteunen de NICE-kwaliteitsnorm voor sepsis. (NICE, 2019)
NICE, het National Institute for Health and Care Excellence, biedt nationale begeleiding en advies in het Verenigd Koninkrijk om gezondheids- en sociale zorg te verbeteren. Hoewel sepsis multifactorieel is en zelden op delfde manier voorkomt was de Guideline Development Group, die richtlijnen maken, van mening dat het gebruik van een eenvoudige, gestructureerde risicobeoordeling clinici kan helpen bij het identificeren van de ernstige ziekten die onmiddellijk een potentieel levensreddende behandeling nodig hebben. Deze richtlijn zorgt ervoor dat patiënten die volgens recente definities als sepsis worden gedefinieerd, minimaal worden beoordeeld als een matig hoog risico. Deze leidraad gaat ook over passende deëscalatie als sepsis onwaarschijnlijk is en breedspectrumantibiotica of ziekenhuisopname niet geschikt zijn. NICE heeft een richtlijn voor de herkenning, diagnose en behandelingen van sepsis bij kinderen en volwassenen. De aanbevelingen zijn gebaseerd op een systematische evaluatie van het beste beschikbare bewijsmateriaal en een expliciete overweging van de kosteneffectiviteit. Wanneer er minimaal bewijs beschikbaar is, zijn de aanbevelingen gebaseerd op de ervaring van de Guideline Development Group en de mening over wat een goede praktijk is. Mensen met sepsis kunnen niet specifieke, niet-lokale presentatie hebben, zoals een zeer ziek gevoel hebben en hoeven niet noodzakelijk koorts te hebben. Besteed bijzondere aandacht aan de zorgen die de patiënt en de familie of verzorgers uiten, zoals een verandering van het gebruikelijk gedrag. Wees extra voorzichtig als mensen geen goede geschiedenis kunnen geven, zoals mensen met een andere taal of met communicatieproblemen. Beoordeel mensen met een vermoedelijke infectie en identificeer:
- de mogelijke besmettingsbron;
- factoren die het risico op sepsis verhogen;
- alle tekenen die een indicatie zijn voor klinische zorg, zoals nieuwe beginnende afwijkingen in gedrag, circulatie of ademhaling.
Als een persoon een infectie heeft en er is klinische bezorgdheid voor mogelijke sepsis, voer dan een gestructureerde beoordeling uit met behulp van de voorgeschiedenis en lichamelijk onderzoek om het risico op ernstige ziekte of overlijden door sepsis te beoordelen. Wees alert op veranderingen in gedrag, in het bijzonder een nieuwe verandering van mentale toestand, zijn een sterke risicofactor voor sterfte. Tachypnoe wordt geassocieerd met een slecht resultaat voor de patiënt en een slechte diagnose van de infectie, vooral omdat pneumonie een veelvoorkomende oorzaak is van sepsis. Extreme waarden van bloeddruk zijn een reden tot klinische bezorgdheid. Bloeddruk moet echter geïnterpreteerd worden in de context van de eerdere bloeddruk van een persoon als deze bekend is. Tachycardie is een risicofactor voor ernstige infecties, sepsis, voor opname op de intensieve zorgenafdeling en voor sterfte. Koorts kan een risicofactor zijn voor sepsis, hoewel sommige studies aantoonden dat een groot deel van de patiënten met sepsis geen verhoogde temperatuur had, dit met name oudere mensen, mensen die een kankerbehandeling krijgen en degene die ernstig ziek zijn met sepsis hebben minder kans om een verhoogde temperatuur te ontwikkelen. Een gemarmerd uiterlijk en cyanose van de huid, de lippen of de tong zijn markers met een hoog risico op ernstige ziekte of overlijden. (Freitag et al., 2016)
Personen die zijn geclassificeerd als personen met een hoog risico op sepsis hebben antibiotica en vloeistoffen nodig en mogelijk ondersteunende zorg. De behandeling moet tijdig worden uitgevoerd en kan gespecialiseerde en kritische zorg vereisen. Gebruik point of care lactaat testen om de vloeistoftherapie en mogelijke betrokkenheid van kritische zorg te begeleiden. Als onderdeel van de eerste beoordeling moet worden gezocht naar een infectiebron, inclusief bronnen die mogelijk een chirurgische drainage nodig hebben. Doelwit testen volgens geschiedenis en onderzoek bijvoorbeeld een urineanalyse voor mensen met een vermoeden van een urineweg sepsis. Beeldvorming van de buik en bekken moet worden overwogen als er geen waarschijnlijke bron wordt geïdentificeerd na klinisch onderzoek en eerste tests. NICE aanbevelingen adviseren om zeker aandacht te schenken aan ‘think sepsis!”, aan sepsis te denken bij elke persoon met een vermoedelijke infectie. (Freitag et al., 2016) De NICE sepsis guidance is hieronder terug te vinden.
Surviving Sepsis Campaign
SSC is een wereldwijd initiatief gericht op het verbeteren van de overleving van patiënten met sepsis en septische shock (Cecconi, M., Evans, L., Levy, M., & Rhodes, A., 2018). Het werd in 2002 gelanceerd door de Society of Critical Care Medicine (SCCM) en de European Society of Intensive Care Medicine (ESICM), met als doel de mortaliteit aan sepsis te verminderen door bewustzijn te vergroten, de diagnose en de behandeling te verbeteren, opleiding geven aan zorgverleners, ontwikkelen van managementrichtlijnen, het implementeren van een prestatieverbeteringsplan en het verbeteren van post-IC zorg. Een belangrijk doel van de campagne was om clinici aan te moedigen symptomen langs het continuüm van SIRS tot sepsis en septische shock te herkennen om vroege identificatie en behandeling van sepsis te vergemakkelijken, waardoor de patiëntuitkomst wordt verbeterd. Het SSC heeft de eerste managementrichtlijnen uitgebracht in 2004 en deze zijn om de vier jaar bijgewerkt. (Makic & Bridges, 2018) De laatste bundel werd uitgebracht in 2018 (Cecconi, M., Evans, L., Levy, M., & Rhodes, A., 2018). De “sepsisbundel” staat centraal in de uitvoering van de Overlevingscampagne (SSC) vanaf de eerste publicatie van de op bewijs gebaseerde richtlijnen in 2004 tot en met de daaropvolgende edities. De bundels vormen sinds 2005 een middel om voorlichting en verbetering te geven met betrekking tot het beheer van sepsis. De literatuur ondersteunt het gebruik van sepsisbundels voor het verbeteren van de resultaten bij patiënten met sepsis en septische shock. Sepsis is een medisch noodgeval, net zoals bij een acuut myocardinfarct, een polytrauma en een beroerte vormt vroege identificatie en passende onmiddellijke behandeling in de eerste uren na de ontwikkeling ervan een betere outcome (Levy et al., 2018; Smyth et al., 2019; Walters, 2018). Hoewel los van de SSC-richtlijnen gepubliceerd, hebben de sepsis-bundelelementen een belangrijke rol gespeeld bij de implementatie van de richtlijnen. Een bundel is een set van individuele evidence based zorgelementen die bij gezamenlijk gebruik een groter bewezen voordeel opleveren dan individueel. (Hassan, E., 2020)
De SSC-bundels zijn ontwikkeld in samenwerking met een educatief en verbeterend partnership met het Instituut voor Verbetering van de Gezondheidszorg. De SSC-bundels die gebaseerd zijn op eerdere richtlijnen zijn aangenomen door het Amerikaanse National Quality Forum en zijn ook aangepast door de regelgevende instanties van het Amerikaanse gezondheidszorgsysteem voor openbare verslaggeving. (Rhodes et al., 2017) Zoals bij de invoering werd opgemerkt, zijn de bundelelementen ontworpen om te worden bijgewerkt naargelang nieuw bewijsmateriaal. In 2018 verscheen er een update van deze bundel. (Levy et al., 2018) In de richtlijnen wordt weergegeven dat patiënten met sepsis dringende moeten worden beoordeeld en behandeld, inclusief de eerste vloeistofresuscitatie, terwijl de broncontrole wordt verder gezet, verdere laboratoriumresultaten worden verkregen en nauwkeuriger metingen van de hemodynamische toestand worden uitgevoerd. Een leidende principe is dat deze complexe patiënten behoefte hebben aan een gedetailleerde eerste beoordeling en vervolgens aan een voortdurende opvolging van de behandeling. (Levy et al., 2018; Walters, 2018)
Herziening van de sepsisbundels
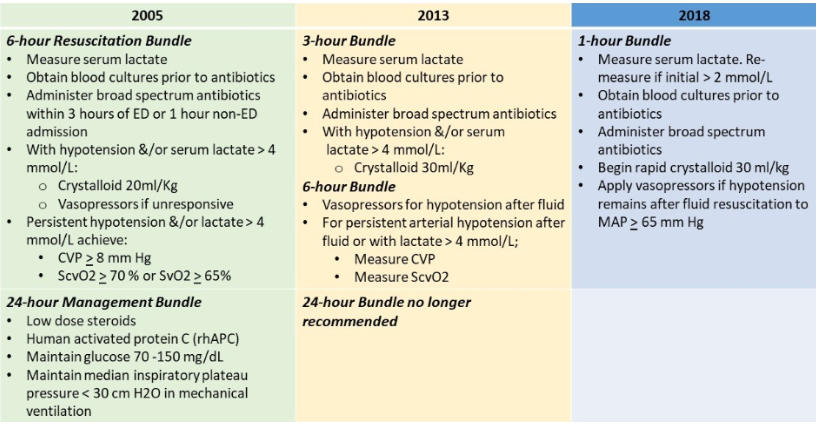
De originele set sepsisbundels bestond uit een resuscitatie (5 elementen) en management (4 elementen) bundelelementen, die respectievelijk binnen 6 en 24 uur moesten worden voltooid. Vanaf het begin werden verschillende aanbevelingen in twijfel getrokken en niet altijd aanvaard met betrekking tot de bewezen waarde. Hoewel de 6- en 24-uursbunels nooit prospectief zijn getest, bleven ze deel uitmaken van de herziene SSC-richtlijnen van 2009. De SSC-herzieningen van 2013 omvatten herzieningen van de bundelelementen na beoordeling van 32.000 patiënten van 239 ziekenhuizen in 17 landen. De resuscitatiebundel werd opgedeeld in tweed delen: een 3 uur durende bundel (4 elementen) en een 6 uur durende bundel (3 elementen). Het meten van centraal veneuze druk (CVD) en centraal veneuze zuurstofverzadiging (ScvO²) zonder specifieke doelen werd aanbevolen als de patiënt niet reageerde op resuscitatie. Naleving van centraal veneuze druk en ScvO² was echter zeer variabel en doorgaans laag, waarbij hun bijdrage aan de vermindering van sterfte twijfelachtig bleef. Kort na deze aanbevelingen toonden aanvullende gegevens aan dat de meting van de CVD en ScvO² niet nodig was voor succesvolle resuscitatie en deze elementen werden verwijderd. Na de SSC-herzieningen van 2018 zijn de bundels van 3 uur en 6 uur gecombineerd tot één bundel van 1 uur (5 elementen). (Hassan, E., 2020)
SSC is een wereldwijd initiatief gericht op het verbeteren van de overleving van patiënten met sepsis en septische shock (Cecconi, M., Evans, L., Levy, M., & Rhodes, A., 2018). Het werd in 2002 gelanceerd door de Society of Critical Care Medicine (SCCM) en de European Society of Intensive Care Medicine (ESICM), met als doel de mortaliteit aan sepsis te verminderen door bewustzijn te vergroten, de diagnose en de behandeling te verbeteren, opleiding geven aan zorgverleners, ontwikkelen van managementrichtlijnen, het implementeren van een prestatieverbeteringsplan en het verbeteren van post-IC zorg. Een belangrijk doel van de campagne was om clinici aan te moedigen symptomen langs het continuüm van SIRS tot sepsis en septische shock te herkennen om vroege identificatie en behandeling van sepsis te vergemakkelijken, waardoor de patiëntuitkomst wordt verbeterd. Het SSC heeft de eerste managementrichtlijnen uitgebracht in 2004 en deze zijn om de vier jaar bijgewerkt. (Makic & Bridges, 2018) De laatste bundel werd uitgebracht in 2018 (Cecconi, M., Evans, L., Levy, M., & Rhodes, A., 2018). De “sepsisbundel” staat centraal in de uitvoering van de Overlevingscampagne (SSC) vanaf de eerste publicatie van de op bewijs gebaseerde richtlijnen in 2004 tot en met de daaropvolgende edities. De bundels vormen sinds 2005 een middel om voorlichting en verbetering te geven met betrekking tot het beheer van sepsis. De literatuur ondersteunt het gebruik van sepsisbundels voor het verbeteren van de resultaten bij patiënten met sepsis en septische shock. Sepsis is een medisch noodgeval, net zoals bij een acuut myocardinfarct, een polytrauma en een beroerte vormt vroege identificatie en passende onmiddellijke behandeling in de eerste uren na de ontwikkeling ervan een betere outcome (Levy et al., 2018; Smyth et al., 2019; Walters, 2018). Hoewel los van de SSC-richtlijnen gepubliceerd, hebben de sepsis-bundelelementen een belangrijke rol gespeeld bij de implementatie van de richtlijnen. Een bundel is een set van individuele evidence based zorgelementen die bij gezamenlijk gebruik een groter bewezen voordeel opleveren dan individueel. (Hassan, E., 2020)
De SSC-bundels zijn ontwikkeld in samenwerking met een educatief en verbeterend partnership met het Instituut voor Verbetering van de Gezondheidszorg. De SSC-bundels die gebaseerd zijn op eerdere richtlijnen zijn aangenomen door het Amerikaanse National Quality Forum en zijn ook aangepast door de regelgevende instanties van het Amerikaanse gezondheidszorgsysteem voor openbare verslaggeving. (Rhodes et al., 2017) Zoals bij de invoering werd opgemerkt, zijn de bundelelementen ontworpen om te worden bijgewerkt naargelang nieuw bewijsmateriaal. In 2018 verscheen er een update van deze bundel. (Levy et al., 2018) In de richtlijnen wordt weergegeven dat patiënten met sepsis dringende moeten worden beoordeeld en behandeld, inclusief de eerste vloeistofresuscitatie, terwijl de broncontrole wordt verder gezet, verdere laboratoriumresultaten worden verkregen en nauwkeuriger metingen van de hemodynamische toestand worden uitgevoerd. Een leidende principe is dat deze complexe patiënten behoefte hebben aan een gedetailleerde eerste beoordeling en vervolgens aan een voortdurende opvolging van de behandeling. (Levy et al., 2018; Walters, 2018)
Herziening van de sepsisbundels
De originele set sepsisbundels bestond uit een resuscitatie (5 elementen) en management (4 elementen) bundelelementen, die respectievelijk binnen 6 en 24 uur moesten worden voltooid. Vanaf het begin werden verschillende aanbevelingen in twijfel getrokken en niet altijd aanvaard met betrekking tot de bewezen waarde. Hoewel de 6- en 24-uursbunels nooit prospectief zijn getest, bleven ze deel uitmaken van de herziene SSC-richtlijnen van 2009. De SSC-herzieningen van 2013 omvatten herzieningen van de bundelelementen na beoordeling van 32.000 patiënten van 239 ziekenhuizen in 17 landen. De resuscitatiebundel werd opgedeeld in tweed delen: een 3 uur durende bundel (4 elementen) en een 6 uur durende bundel (3 elementen). Het meten van centraal veneuze druk (CVD) en centraal veneuze zuurstofverzadiging (ScvO²) zonder specifieke doelen werd aanbevolen als de patiënt niet reageerde op resuscitatie. Naleving van centraal veneuze druk en ScvO² was echter zeer variabel en doorgaans laag, waarbij hun bijdrage aan de vermindering van sterfte twijfelachtig bleef. Kort na deze aanbevelingen toonden aanvullende gegevens aan dat de meting van de CVD en ScvO² niet nodig was voor succesvolle resuscitatie en deze elementen werden verwijderd. Na de SSC-herzieningen van 2018 zijn de bundels van 3 uur en 6 uur gecombineerd tot één bundel van 1 uur (5 elementen). (Hassan, E., 2020)
1-Hour bundel
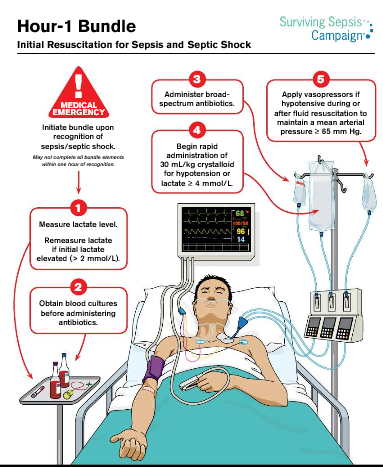
De nieuwe sepsis bundel is gebaseerd op de richtlijnen van 2016. Consistent met eerder iteraties van de SSC sepsisbundels is dat “time zero” of “time of presentation” wordt gedefinieerd als het tijdstip van triage op de spoedgevallendienst of, indien verwezen vanaf een andere zorglocatie, vanaf de vroegste kenmerken die overeenkomt met de aspecten van sepsis of septische shock. De belangrijkste verandering in de herziening van de SSC-bundels is dat de 3-uur en 6-uur bundels zijn gecombineerd in een "1-uur bundel" met de expliciete intentie om onmiddellijk te beginnen met resuscitatie en management. Er moet onmiddellijk begonnen worden met de behandeling, vooral bij patiënten met hypotensie, in plaats van te wachten en de resuscitatiemaatregelen uit te breiden of te verlengen over een langere periode. Het is mogelijk dat er meer dan één uur nodig is voor de resuscitatie af te ronden maar de start van resuscitatie en behandeling, zoals een bloedname voor het meten van lactaat en hemoculturen, toediening van vloeistoffen en antibiotica, en in het geval van levensbedreigende hypotensie, initiatie van vasopressortherapie, moeten onmiddellijk gestart worden. (Levy et al., 2018).
De nieuwe sepsis bundel is gebaseerd op de richtlijnen van 2016. Consistent met eerder iteraties van de SSC sepsisbundels is dat “time zero” of “time of presentation” wordt gedefinieerd als het tijdstip van triage op de spoedgevallendienst of, indien verwezen vanaf een andere zorglocatie, vanaf de vroegste kenmerken die overeenkomt met de aspecten van sepsis of septische shock. De belangrijkste verandering in de herziening van de SSC-bundels is dat de 3-uur en 6-uur bundels zijn gecombineerd in een "1-uur bundel" met de expliciete intentie om onmiddellijk te beginnen met resuscitatie en management. Er moet onmiddellijk begonnen worden met de behandeling, vooral bij patiënten met hypotensie, in plaats van te wachten en de resuscitatiemaatregelen uit te breiden of te verlengen over een langere periode. Het is mogelijk dat er meer dan één uur nodig is voor de resuscitatie af te ronden maar de start van resuscitatie en behandeling, zoals een bloedname voor het meten van lactaat en hemoculturen, toediening van vloeistoffen en antibiotica, en in het geval van levensbedreigende hypotensie, initiatie van vasopressortherapie, moeten onmiddellijk gestart worden. (Levy et al., 2018).
Lactaat
Hoewel serumlactaat geen directe meeting is van weefselhypoperfusie, geeft het toch een goed beeld over de weefselperfusie. Als het lactaat stijgt, kan dit wijzen op weefselhypoxie, versnelde aërobe glycolyse veroorzaakt door een overtollige beta-adrenerge stimulatie, of andere oorzaken die verband houden met slechtere perfusie. Verscheidene onderzoeken hebben aangetoond dat lactaatgestuurde resuscitatie een lagere mortaliteit kent. Bij een hyperlactatemie van > 2 mmol/l is er een nieuwe meting nodig binnen de 2-4 uur. Op deze manier wordt de resuscitatie verricht op geleide van het lactaatgehalte. (Levy et al., 2018)
Hemoculturen voor toediening antibiotica
Culturen kunnen reeds gesteriliseerd worden binnen enkele minuten na antibiotica inname, op voorwaarde dat deze de juiste antimicrobiële stof is. Daarom is het aangeraden dat de hemoculturen voor toediening van de antibiotica worden afgenomen. Op deze manier kunnen de ziekteverwerkers correct geïdentificeerd worden. Er dienen minstens twee sets hemoculturen afgenomen te worden, zowel aëroob als anaëroob. De afname van deze culturen mag geen vertraging veroorzaken in de antibioticatherapie. (Levy et al., 2018)
Antibiotica
Er wordt de voorkeur gegeven aan een breedspectrum-antibioticum. Deze heeft meerdere antimicrobiële stoffen waardoor de kans groter is dat de ziekteverwekker wordt bestreden. De antibioticatherapie moet onmiddellijk gestart worden, bij voorkeur na afname van de hemoculturen. Deze afname mag geen reden zijn om de start van de antibioticatherapie uit te stellen. Van zodra de resultaten van de hemoculturen bekend zijn en de ziekteverwekker gekend is, zal er gerichter antibiotica gegeven worden. Indien blijkt dat de patiënt geen infectie heeft, zal de antibioticatherapie worden stopgezet. (Levy et al., 2018)
Vochtresuscitatie
Vroege vochtresuscitatie is cruciaal voor de stabilisatie van sepsis-geïnduceerde weefselhypoperfusie of septische shock. Van zodra sepsis bij een patiënt wordt herkend en/of er hypotensie en een verhoogd lactaat wordt vastgesteld, is het noodzakelijk dat er na herkenning een vochtbolus wordt gegeven. Deze moet onmiddellijk gestart worden en dient volledig toegediend te zijn binnen drie uren. In de richtlijnen wordt aanbevolen om een minimum van 30ml/kg intraveneuze kristalloïde te gebruiken. Hoewel weinig literatuur gecontroleerde gegevens bevat om dit volume te ondersteunen, hebben recente interventiestudies dit beschreven als gebruikelijke praktijk in de vroege stadia van resuscitatie en observationeel bewijs is ondersteunend. Omwille van een ontbrekend duidelijk voordeel na toediening van colloïde oplossingen in vergelijking met kristalloïde oplossingen en op basis van de kosten, ondersteunt een sterke aanbeveling voor het gebruik van kristalloïde infuusvloeistoffen. Na elke vochtbolus moet er nagegaan worden of de patiënt nog steeds vochtontvankelijk is. (Levy et al., 2018)
Vasopressie
Het is zeer belangrijk dat de perfusiedruk naar de organen zo snel mogelijk hersteld wordt. Als de bloeddruk niet hersteld is na de eerste vochtbolus, dan moet er vasopressie opgestart worden binnen het eerste uur zodat er een MAP bereikt wordt van ≥65 mmHg. (Levy et al., 2018)
Hoewel serumlactaat geen directe meeting is van weefselhypoperfusie, geeft het toch een goed beeld over de weefselperfusie. Als het lactaat stijgt, kan dit wijzen op weefselhypoxie, versnelde aërobe glycolyse veroorzaakt door een overtollige beta-adrenerge stimulatie, of andere oorzaken die verband houden met slechtere perfusie. Verscheidene onderzoeken hebben aangetoond dat lactaatgestuurde resuscitatie een lagere mortaliteit kent. Bij een hyperlactatemie van > 2 mmol/l is er een nieuwe meting nodig binnen de 2-4 uur. Op deze manier wordt de resuscitatie verricht op geleide van het lactaatgehalte. (Levy et al., 2018)
Hemoculturen voor toediening antibiotica
Culturen kunnen reeds gesteriliseerd worden binnen enkele minuten na antibiotica inname, op voorwaarde dat deze de juiste antimicrobiële stof is. Daarom is het aangeraden dat de hemoculturen voor toediening van de antibiotica worden afgenomen. Op deze manier kunnen de ziekteverwerkers correct geïdentificeerd worden. Er dienen minstens twee sets hemoculturen afgenomen te worden, zowel aëroob als anaëroob. De afname van deze culturen mag geen vertraging veroorzaken in de antibioticatherapie. (Levy et al., 2018)
Antibiotica
Er wordt de voorkeur gegeven aan een breedspectrum-antibioticum. Deze heeft meerdere antimicrobiële stoffen waardoor de kans groter is dat de ziekteverwekker wordt bestreden. De antibioticatherapie moet onmiddellijk gestart worden, bij voorkeur na afname van de hemoculturen. Deze afname mag geen reden zijn om de start van de antibioticatherapie uit te stellen. Van zodra de resultaten van de hemoculturen bekend zijn en de ziekteverwekker gekend is, zal er gerichter antibiotica gegeven worden. Indien blijkt dat de patiënt geen infectie heeft, zal de antibioticatherapie worden stopgezet. (Levy et al., 2018)
Vochtresuscitatie
Vroege vochtresuscitatie is cruciaal voor de stabilisatie van sepsis-geïnduceerde weefselhypoperfusie of septische shock. Van zodra sepsis bij een patiënt wordt herkend en/of er hypotensie en een verhoogd lactaat wordt vastgesteld, is het noodzakelijk dat er na herkenning een vochtbolus wordt gegeven. Deze moet onmiddellijk gestart worden en dient volledig toegediend te zijn binnen drie uren. In de richtlijnen wordt aanbevolen om een minimum van 30ml/kg intraveneuze kristalloïde te gebruiken. Hoewel weinig literatuur gecontroleerde gegevens bevat om dit volume te ondersteunen, hebben recente interventiestudies dit beschreven als gebruikelijke praktijk in de vroege stadia van resuscitatie en observationeel bewijs is ondersteunend. Omwille van een ontbrekend duidelijk voordeel na toediening van colloïde oplossingen in vergelijking met kristalloïde oplossingen en op basis van de kosten, ondersteunt een sterke aanbeveling voor het gebruik van kristalloïde infuusvloeistoffen. Na elke vochtbolus moet er nagegaan worden of de patiënt nog steeds vochtontvankelijk is. (Levy et al., 2018)
Vasopressie
Het is zeer belangrijk dat de perfusiedruk naar de organen zo snel mogelijk hersteld wordt. Als de bloeddruk niet hersteld is na de eerste vochtbolus, dan moet er vasopressie opgestart worden binnen het eerste uur zodat er een MAP bereikt wordt van ≥65 mmHg. (Levy et al., 2018)