Sepsis is een tijdgevoelige aandoening. Een snellere diagnose van sepsis zou de mortaliteit, de duur van het ziekenhuisverblijf kunnen verkorten en de kosten hieraan verbonden kunnen verlagen. (Coopersmith et al., 2018) Zoals reeds eerder aangehaald is sepsis geen duidelijk gedefinieerde ziekte, maar eerder een klinisch syndroom dat wordt gedefinieerd door een combinatie van tekenen, symptomen, laboratoriumafwijkingen en orgaanstoornissen. Sepsis is moeilijk te diagnosticeren, moeilijker te controleren en uniforme strategieën voor quarantaine zijn niet van toepassing. (Hotchkiss et al., 2017; Kempker et al., 2018)
Van zodra een patiënt positief wordt getrieerd op sepsis, dat wil zeggen dat er een vermoeden is van sepsis, zal deze patiënt gemonitord worden en zullen er verscheidene onderzoeken gebeuren om sepsis te kunnen diagnosticeren en te onderscheiden van andere aandoeningen. Zo wordt de orgaanfunctie (bijvoorbeeld nier- en leverfunctie), oxygenatie en het zuur-base evenwicht onderzocht aan de hand van een bloedname en het lactaatgehalte gemeten binnen het uur na aankomst. Het is bewezen dat dit geassocieerd wordt met een betere outcome.
Er worden ook steeds hemoculturen afgenomen. Bij voorkeur voor toediening van antibiotica omdat de kweken reeds gesteriliseerd kunnen zijn enkele minuten na toediening van antibiotica. Er dienen steeds twee sets hemoculturen afgenomen te worden (aëroob en anaëroob). Het afnemen van deze sets mogen de behandeling niet vertragen maar het optimaliseren van de identificatie van pathogenen om de outcome te verbeteren is van cruciaal belang. Hemoculturen zijn niet steeds positief, enerzijds omdat bacteriën niet in de bloedbaan hoeven te circuleren om sepsis te veroorzaken en anderzijds omdat patiënten soms al met antibiotica worden behandeld op het moment dat deze culturen worden afgenomen. Diagnose op basis van culturen verloopt langzamer dan een diagnose die gesteld wordt aan de hand van biomarkers, zoals C-reactief eiwit (CRP) en procalcitonine (PCT). Vaak duurt het een tweetal dagen, soms wel zeven dagen vooraleer de resultaten van hemoculturen bekend zijn. Biomarkers alleen zijn niet voldoende voor een diagnose maar vormen wel een goede aanvulling op een klinische beoordeling van andere laboratoriumgegeven. Bijkomend wordt er ook een electrocardiogram en een urine-en sputumstaal afgenomen. Deze onderzoeken dienen zo snel mogelijk uitgevoerd te worden. (Charitos, Topi, Castellaneta, & D’ Agostino, 2019; Coopersmith et al., 2018; Hotchkiss et al., 2017; Rello et al., 2017; Society of Critical Care Medicine, 2019) De verschillende organen worden ook onderzocht. Complicaties moeten opgespoord worden en de infectiehaard moet bepaald worden, dit kan aan de hand van beeldvorming (röntgenstralen, CT-scans of echografieën). (Rello et al., 2017)
Pro-inflammatoire biomarkers
C-reactief Eiwit
C-reactief eiwit (CRP) is een acuut-fase-eiwit dat wordt geproduceerd door de lever, het kan ook gesynthetiseerd worden door andere cellen zoals alveolaire macrofagen. De plasmaconcentratie blijft stabiel bij gezonde patiënten maar kan stijgen na trauma, ontsteking en andere stimuli met betrekking tot weefselschade. Bacteriële infecties veroorzaken een snelle stijging van het CRP. Veranderingen in de plasmaspiegels van CRP kunnen nuttig zijn bij de diagnose en prognose van een infectie; een daling van de plasmaspiegels geeft aan dat de infectie is opgelost. Zijn korte halfwaardetijd van ongeveer 19u. maakt dat CRP een nuttig hulpmiddel is in het toezicht op de ontstekingsreactie, de besmetting, en de antibiotische therapie. (Rello et al., 2017)
In tegenstelling tot de meeste acute-fase-eiwitten, die grote variaties in de plasmaspiegels ondergaan (afhankelijk van de mate van synthese, consumptie en katabolisme), blijven de CRP-plasmaspiegels vrijwel constant. Zij worden dus bepaald door de snelheid van synthese en hun waarden weerspiegelen de aanwezigheid en de omvang van de ziekte. Onderzoek van Miglietta et al. heeft de incidentie van orgaanfalen bij septische patiënten gelinkt aan de ernst van de klinische toestand en met de intensiteit van de ontstekingsstimulus waarbij een verband gevonden is tussen CRP niveaus en de incidentie van orgaanfalen. Het lijkt erop dat de CRP plasmaconcentratie de omvang van de ontstekingsstimulus en ernst van de sepsis reflecteert. (Rello et al., 2017)
Geïsoleerde CRP-waarden kunnen dus nuttig zijn bij de diagnose van sepsis. In de klinische praktijk zijn seriële metingen echter nuttiger om de respons van de patiënt te controleren. CRP is vrij onspecifiek en het onderscheidt geen sepsis van andere ziekten. Het wordt echter wel vaak gebruikt om te screenen naar sepsis bij neonaten omdat de gevoeligheid zeer hoog is. Deze is ook hoog na een operatie en wordt dus ook gebruikt om patiënten postoperatief te controleren. (Rello et al., 2017)
Procalcitonine
Procalcitonine (PCT) wordt wereldwijd beschouwd als de meest bruikbare marker voor ernstige systemische infecties. In normale omstandigheden is dit in zeer kleine hoeveelheden aanwezig in het bloed. De productie ervan kan gestimuleerd worden door ontstekingscytokines en bacteriële endotoxines. Er worden dan grotere hoeveelheden PCT vrijgegeven in reactie op de infectie, in het bijzonder op bacteriële infecties. In vergelijking met andere beschikbare sepsismarkers, heeft PCT ook de mogelijkheid om een onderscheid te maken tussen besmettelijke en niet-besmettelijke infecties en tussen virale en bacteriële infecties. Het kan ook wijzen op een bacteriële surinfectie bij patiënten met een virale infectie. (Rello et al., 2017)
De hoeveelheid PCT in het bloed dient dus als een marker voor een inflammatoire reactie, welke een indicator is op het risico van sepsis. Hoe groter de hoeveelheid PCT, hoe groter het risico op een systemische infectie en sepsis. Gezien zijn hoge gevoeligheid voor de meeste soorten infecties, wordt PCT beschouwd als de gevoeligste biomarker om bacteriële sepsis te diagnosticeren of uit te sluiten. De globale richtlijnen adviseren ook het gebruik hiervan als hulpmiddel om antibiotische behandeling te optimaliseren. Het heeft een kortere halfwaardetijd dan CRP en de PCT niveaus stijgen eerder bij bacteriële besmetting. Hierdoor kan sepsis vroeger gediagnosticeerd worden en kan de vooruitgang beter gecontroleerd worden. (Rello et al., 2017)
De Federatie Medisch Specialisten beveelt dan weer aan om CRP te gebruiken bij verdenking van sepsis om een infectie meer of minder waarschijnlijker te maken. PCT heeft volgens hen geen meerwaarde gezien de hogere kosten voor het bepalen van deze biomarker. (Specialisten, 2020)
Biomarkers van orgaanfalen
Lactaat
Lactaat is de beste marker voor een slechte weefselperfusie. Toename van het serumlactaatgehalte wijst op een ontwikkeling naar een orgaandisfunctie en gaat gepaard met een verhoogd sterftecijfer van 35% tot 70%. Om deze reden wordt een hoog lactaat dan ook beschouwd als een sepsis marker. (Rello et al., 2017; Shetty et al., 2018)
Verscheidene studies hebben het gebruik van lactaat als marker voor diagnose, prognose en behandeling van weefselhypoxie tijdens shock vastgesteld. In het algemeen is de bepaling van lactaat een onbetwistbaar criterium in de risicostratificatie van septische patiënten en geeft het advies over het gebruik van vasoactieve medicatie. De omvang van de hyperlactatemie reflecteert de ernst van de hypoperfusie en is direct verwant met mortaliteit. Een patiënt met ernstige sepsis in combinatie met een significante hypoperfusie (lactaat > 4 mmol/l) wordt beschouwd in shock te zijn zelfs indien deze patiënt niet voldoet aan de hypotensiecriteria. Normotensieve patiënten met ernstige sepsis en een significante lactaatacidose moeten snel antibiotica en een adequate vochtresuscitatie krijgen alsook hemodynamische controle. (Rello et al., 2017)
Bij meer dan 10% van de patiënten met een lactaat > 2 mmol/l veroorzaakt de hyperlactatemie een negatieve uitkomst zoals een verblijf op de intensieve zorgen van minstens 72u of in hospitaal overlijden. (Shetty et al., 2018)
Lactaat wordt ook gebruikt als een prognostische marker, een indicator voor de ernst van sepsis. Het niet kunnen klaren van lactaat in het bloed, kan wijzen op een nakende dood. Bij sepsis kan een verhoogd lactaatniveau te wijten zijn aan een veranderde klaring, overproductie of een combinatie van beide. Een hoog lactaatniveau kan dus wijzen op een orgaandisfunctie, aangezien de klaring hiervan afhankelijk is van de lever- en nierfunctie. (Rello et al., 2017)
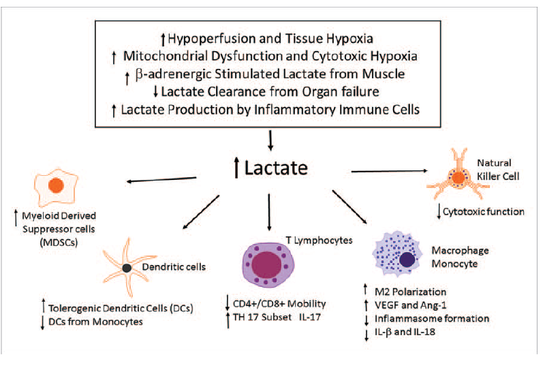
Recente studies van Leite et al., Haas et al., Choi et al. suggereren zelfs dat lactaat een immunosuppresief effect kan hebben in zijn lokale omgeving. Voor de activering van immuuncellen is een aërobe glycolytische stofwisseling nodig welke lactaat produceert. (Nolt et al., 2018)
Van zodra een patiënt positief wordt getrieerd op sepsis, dat wil zeggen dat er een vermoeden is van sepsis, zal deze patiënt gemonitord worden en zullen er verscheidene onderzoeken gebeuren om sepsis te kunnen diagnosticeren en te onderscheiden van andere aandoeningen. Zo wordt de orgaanfunctie (bijvoorbeeld nier- en leverfunctie), oxygenatie en het zuur-base evenwicht onderzocht aan de hand van een bloedname en het lactaatgehalte gemeten binnen het uur na aankomst. Het is bewezen dat dit geassocieerd wordt met een betere outcome.
Er worden ook steeds hemoculturen afgenomen. Bij voorkeur voor toediening van antibiotica omdat de kweken reeds gesteriliseerd kunnen zijn enkele minuten na toediening van antibiotica. Er dienen steeds twee sets hemoculturen afgenomen te worden (aëroob en anaëroob). Het afnemen van deze sets mogen de behandeling niet vertragen maar het optimaliseren van de identificatie van pathogenen om de outcome te verbeteren is van cruciaal belang. Hemoculturen zijn niet steeds positief, enerzijds omdat bacteriën niet in de bloedbaan hoeven te circuleren om sepsis te veroorzaken en anderzijds omdat patiënten soms al met antibiotica worden behandeld op het moment dat deze culturen worden afgenomen. Diagnose op basis van culturen verloopt langzamer dan een diagnose die gesteld wordt aan de hand van biomarkers, zoals C-reactief eiwit (CRP) en procalcitonine (PCT). Vaak duurt het een tweetal dagen, soms wel zeven dagen vooraleer de resultaten van hemoculturen bekend zijn. Biomarkers alleen zijn niet voldoende voor een diagnose maar vormen wel een goede aanvulling op een klinische beoordeling van andere laboratoriumgegeven. Bijkomend wordt er ook een electrocardiogram en een urine-en sputumstaal afgenomen. Deze onderzoeken dienen zo snel mogelijk uitgevoerd te worden. (Charitos, Topi, Castellaneta, & D’ Agostino, 2019; Coopersmith et al., 2018; Hotchkiss et al., 2017; Rello et al., 2017; Society of Critical Care Medicine, 2019) De verschillende organen worden ook onderzocht. Complicaties moeten opgespoord worden en de infectiehaard moet bepaald worden, dit kan aan de hand van beeldvorming (röntgenstralen, CT-scans of echografieën). (Rello et al., 2017)
Pro-inflammatoire biomarkers
C-reactief Eiwit
C-reactief eiwit (CRP) is een acuut-fase-eiwit dat wordt geproduceerd door de lever, het kan ook gesynthetiseerd worden door andere cellen zoals alveolaire macrofagen. De plasmaconcentratie blijft stabiel bij gezonde patiënten maar kan stijgen na trauma, ontsteking en andere stimuli met betrekking tot weefselschade. Bacteriële infecties veroorzaken een snelle stijging van het CRP. Veranderingen in de plasmaspiegels van CRP kunnen nuttig zijn bij de diagnose en prognose van een infectie; een daling van de plasmaspiegels geeft aan dat de infectie is opgelost. Zijn korte halfwaardetijd van ongeveer 19u. maakt dat CRP een nuttig hulpmiddel is in het toezicht op de ontstekingsreactie, de besmetting, en de antibiotische therapie. (Rello et al., 2017)
In tegenstelling tot de meeste acute-fase-eiwitten, die grote variaties in de plasmaspiegels ondergaan (afhankelijk van de mate van synthese, consumptie en katabolisme), blijven de CRP-plasmaspiegels vrijwel constant. Zij worden dus bepaald door de snelheid van synthese en hun waarden weerspiegelen de aanwezigheid en de omvang van de ziekte. Onderzoek van Miglietta et al. heeft de incidentie van orgaanfalen bij septische patiënten gelinkt aan de ernst van de klinische toestand en met de intensiteit van de ontstekingsstimulus waarbij een verband gevonden is tussen CRP niveaus en de incidentie van orgaanfalen. Het lijkt erop dat de CRP plasmaconcentratie de omvang van de ontstekingsstimulus en ernst van de sepsis reflecteert. (Rello et al., 2017)
Geïsoleerde CRP-waarden kunnen dus nuttig zijn bij de diagnose van sepsis. In de klinische praktijk zijn seriële metingen echter nuttiger om de respons van de patiënt te controleren. CRP is vrij onspecifiek en het onderscheidt geen sepsis van andere ziekten. Het wordt echter wel vaak gebruikt om te screenen naar sepsis bij neonaten omdat de gevoeligheid zeer hoog is. Deze is ook hoog na een operatie en wordt dus ook gebruikt om patiënten postoperatief te controleren. (Rello et al., 2017)
Procalcitonine
Procalcitonine (PCT) wordt wereldwijd beschouwd als de meest bruikbare marker voor ernstige systemische infecties. In normale omstandigheden is dit in zeer kleine hoeveelheden aanwezig in het bloed. De productie ervan kan gestimuleerd worden door ontstekingscytokines en bacteriële endotoxines. Er worden dan grotere hoeveelheden PCT vrijgegeven in reactie op de infectie, in het bijzonder op bacteriële infecties. In vergelijking met andere beschikbare sepsismarkers, heeft PCT ook de mogelijkheid om een onderscheid te maken tussen besmettelijke en niet-besmettelijke infecties en tussen virale en bacteriële infecties. Het kan ook wijzen op een bacteriële surinfectie bij patiënten met een virale infectie. (Rello et al., 2017)
De hoeveelheid PCT in het bloed dient dus als een marker voor een inflammatoire reactie, welke een indicator is op het risico van sepsis. Hoe groter de hoeveelheid PCT, hoe groter het risico op een systemische infectie en sepsis. Gezien zijn hoge gevoeligheid voor de meeste soorten infecties, wordt PCT beschouwd als de gevoeligste biomarker om bacteriële sepsis te diagnosticeren of uit te sluiten. De globale richtlijnen adviseren ook het gebruik hiervan als hulpmiddel om antibiotische behandeling te optimaliseren. Het heeft een kortere halfwaardetijd dan CRP en de PCT niveaus stijgen eerder bij bacteriële besmetting. Hierdoor kan sepsis vroeger gediagnosticeerd worden en kan de vooruitgang beter gecontroleerd worden. (Rello et al., 2017)
De Federatie Medisch Specialisten beveelt dan weer aan om CRP te gebruiken bij verdenking van sepsis om een infectie meer of minder waarschijnlijker te maken. PCT heeft volgens hen geen meerwaarde gezien de hogere kosten voor het bepalen van deze biomarker. (Specialisten, 2020)
Biomarkers van orgaanfalen
Lactaat
Lactaat is de beste marker voor een slechte weefselperfusie. Toename van het serumlactaatgehalte wijst op een ontwikkeling naar een orgaandisfunctie en gaat gepaard met een verhoogd sterftecijfer van 35% tot 70%. Om deze reden wordt een hoog lactaat dan ook beschouwd als een sepsis marker. (Rello et al., 2017; Shetty et al., 2018)
Verscheidene studies hebben het gebruik van lactaat als marker voor diagnose, prognose en behandeling van weefselhypoxie tijdens shock vastgesteld. In het algemeen is de bepaling van lactaat een onbetwistbaar criterium in de risicostratificatie van septische patiënten en geeft het advies over het gebruik van vasoactieve medicatie. De omvang van de hyperlactatemie reflecteert de ernst van de hypoperfusie en is direct verwant met mortaliteit. Een patiënt met ernstige sepsis in combinatie met een significante hypoperfusie (lactaat > 4 mmol/l) wordt beschouwd in shock te zijn zelfs indien deze patiënt niet voldoet aan de hypotensiecriteria. Normotensieve patiënten met ernstige sepsis en een significante lactaatacidose moeten snel antibiotica en een adequate vochtresuscitatie krijgen alsook hemodynamische controle. (Rello et al., 2017)
Bij meer dan 10% van de patiënten met een lactaat > 2 mmol/l veroorzaakt de hyperlactatemie een negatieve uitkomst zoals een verblijf op de intensieve zorgen van minstens 72u of in hospitaal overlijden. (Shetty et al., 2018)
Lactaat wordt ook gebruikt als een prognostische marker, een indicator voor de ernst van sepsis. Het niet kunnen klaren van lactaat in het bloed, kan wijzen op een nakende dood. Bij sepsis kan een verhoogd lactaatniveau te wijten zijn aan een veranderde klaring, overproductie of een combinatie van beide. Een hoog lactaatniveau kan dus wijzen op een orgaandisfunctie, aangezien de klaring hiervan afhankelijk is van de lever- en nierfunctie. (Rello et al., 2017)
Recente studies van Leite et al., Haas et al., Choi et al. suggereren zelfs dat lactaat een immunosuppresief effect kan hebben in zijn lokale omgeving. Voor de activering van immuuncellen is een aërobe glycolytische stofwisseling nodig welke lactaat produceert. (Nolt et al., 2018)
Veneuze naar arteriële koolstofdioxide drukverschil (∆pCO2)
Het anaëroob metabolisme is cruciaal in de pathofysiologie van septische shock. Patiënten met sepsis kunnen gemonitord worden aan de hand van lactaat en ∆pCO2. Koolstofdioxide (CO2) wordt geproduceerd in weefsels tijdens de aërobe en anaërobe stofwisseling. Tijdens de aërobe stofwisseling wordt de hoeveelheid geproduceerde CO2 bepaald door het basale metabolisme en het ademhalingsquotiënt. Tijdens de anaërobe stofwisseling wordt CO2 dan weer geproduceerd uit bicarbonaat dat zure metabolieten buffert. Omdat CO2 ongeveer 20 keer beter oplosbaar is dan zuurstof, is het waarschijnlijker dat deze buiten de ischemische weefsels beschikbaar is voor de veneuze stroom. Dit maakt dat CO2 een gevoelige marker is voor hypoperfusie. Het is daarom dat de meting van ∆pCO2 een goede marker lijkt voor een correcte microcirculatie en een goede prognostische indicator voor septische shock omdat het een index van weefseloxygenatie geeft. ∆pCO2, hetzij uit gemengd of centraal veneus bloed, wordt beschouwd als een predictieve factor voor de capaciteit van het cardiovasculaire systeem om de CO2 geproduceerd in perifere weefsels te elimineren. Hoeveelheden boven 6 mmHg binnen de eerste 24 uur bij ernstig zieke patiënten worden geassocieerd met een slechte afloop. Het nut van deze parameter moet echter nog worden onderzocht. (Rello et al., 2017)
Trombocyten
Hematologisch falen komt vaak voor bij patiënten met septische shock. Trombocytopenie (< 50 000/L) is een sterk negatieve prognostische marker bij sepsis patiënten. Dit zou het gevolg zijn van de activering en verbruik van trombocyten. Verschillende markers voor trombocytenfunctie werden gesuggereerd als biomarkers voor sepsis. Er werd aangetoond dat deze correleren met de ernst van de ziekte. (Greco, Lupia, Bosco, Vizio, & Montrucchio, 2017)
Trombocyten spelen een belangrijke rol bij hemostase en coagulatie. Hoewel hemorragische complicaties tijdens sepsis eerder zeldzaam zijn en zelden leiden tot de dood, is er toch aandacht besteed aan hun rol gericht op het immuunsysteem. Trombocyten zijn in staat om cytokines vrij te geven, leucocyten te recruteren, hebben een interactie met bacteriën en het endotheel en dragen bij tot de vorming van microthrombi. Deze mechanismen zijn flexibel en beschermend in een situatie van een lokale infectie, maar worden ontregeld en "maladaptief" tijdens sepsis, wat bijdraagt aan orgaanschade. (Greco et al., 2017)
Geactiveerde trombocyten staan in wisselwerking met andere cellen via twee hoofdmechanismen; expressie van receptoren op het celoppervlak en het vrijkomen van cytoplasmatische korrels die immunomodulerende proteïnen bevatten. (Greco et al., 2017)
De hechting tussen trombocyten en endotheel en trombocyten-leucocytenaggregatie dragen bij aan de vorming van microthrombi in de kleine vaten. De betrokken cellen geven cytokinen en chemokinen vrij en zorgen zo voor een verdere cellulaire rekrutering. Deze pathologische zelfvoorzienende disfunctie resulteert in een septische shock. De vorming van microthrombi in de vaten veroorzaakt door de ontstekingsreactie en de daaropvolgende rekrutering van immuuncellen en trombocyten staat bekend als immunotrombose. Dit draagt bij aan microvasculaire disfunctie en is een kenmerk van orgaanschade bij sepsis. (Greco et al., 2017)
Capillairen, arteriolen, venen en microlymfevaten maken allemaal deel uit van het microvasculair netwerk. Bij sepsis, zelfs wanneer de orgaanperfusie behouden blijft, zijn er vlekkerige gebieden van verminderde zuurstoftoevoer en -afvoer en functioneel shunting aangetoond. (Greco et al., 2017)
Leukocyten en trombocytenrecrutering, intravasculaire stolling, endotheel schade, verlies van surfactant, oxidatieve stress zijn allemaal mechanismen die mede ernstige longschade verzaken bij sepsis. Post mortem biopsies van patiënten die stierven met ARDS hebben een overmaat aan trombocyten en neutrofielen aangetoond in de pulmonale bloedvaten. De literatuur beschrijft verschillende rollen voor trombocyten in de pathogenese van ARDS. Er werd aangetoond dat uitputting van de trombocyten correleert met een verminderde rekrutering van neutrofielen en dat een verhoogde hoeveelheid trombocyten correleert met een verhoogde neutrofiele activering. (Greco et al., 2017)
Het anaëroob metabolisme is cruciaal in de pathofysiologie van septische shock. Patiënten met sepsis kunnen gemonitord worden aan de hand van lactaat en ∆pCO2. Koolstofdioxide (CO2) wordt geproduceerd in weefsels tijdens de aërobe en anaërobe stofwisseling. Tijdens de aërobe stofwisseling wordt de hoeveelheid geproduceerde CO2 bepaald door het basale metabolisme en het ademhalingsquotiënt. Tijdens de anaërobe stofwisseling wordt CO2 dan weer geproduceerd uit bicarbonaat dat zure metabolieten buffert. Omdat CO2 ongeveer 20 keer beter oplosbaar is dan zuurstof, is het waarschijnlijker dat deze buiten de ischemische weefsels beschikbaar is voor de veneuze stroom. Dit maakt dat CO2 een gevoelige marker is voor hypoperfusie. Het is daarom dat de meting van ∆pCO2 een goede marker lijkt voor een correcte microcirculatie en een goede prognostische indicator voor septische shock omdat het een index van weefseloxygenatie geeft. ∆pCO2, hetzij uit gemengd of centraal veneus bloed, wordt beschouwd als een predictieve factor voor de capaciteit van het cardiovasculaire systeem om de CO2 geproduceerd in perifere weefsels te elimineren. Hoeveelheden boven 6 mmHg binnen de eerste 24 uur bij ernstig zieke patiënten worden geassocieerd met een slechte afloop. Het nut van deze parameter moet echter nog worden onderzocht. (Rello et al., 2017)
Trombocyten
Hematologisch falen komt vaak voor bij patiënten met septische shock. Trombocytopenie (< 50 000/L) is een sterk negatieve prognostische marker bij sepsis patiënten. Dit zou het gevolg zijn van de activering en verbruik van trombocyten. Verschillende markers voor trombocytenfunctie werden gesuggereerd als biomarkers voor sepsis. Er werd aangetoond dat deze correleren met de ernst van de ziekte. (Greco, Lupia, Bosco, Vizio, & Montrucchio, 2017)
Trombocyten spelen een belangrijke rol bij hemostase en coagulatie. Hoewel hemorragische complicaties tijdens sepsis eerder zeldzaam zijn en zelden leiden tot de dood, is er toch aandacht besteed aan hun rol gericht op het immuunsysteem. Trombocyten zijn in staat om cytokines vrij te geven, leucocyten te recruteren, hebben een interactie met bacteriën en het endotheel en dragen bij tot de vorming van microthrombi. Deze mechanismen zijn flexibel en beschermend in een situatie van een lokale infectie, maar worden ontregeld en "maladaptief" tijdens sepsis, wat bijdraagt aan orgaanschade. (Greco et al., 2017)
Geactiveerde trombocyten staan in wisselwerking met andere cellen via twee hoofdmechanismen; expressie van receptoren op het celoppervlak en het vrijkomen van cytoplasmatische korrels die immunomodulerende proteïnen bevatten. (Greco et al., 2017)
De hechting tussen trombocyten en endotheel en trombocyten-leucocytenaggregatie dragen bij aan de vorming van microthrombi in de kleine vaten. De betrokken cellen geven cytokinen en chemokinen vrij en zorgen zo voor een verdere cellulaire rekrutering. Deze pathologische zelfvoorzienende disfunctie resulteert in een septische shock. De vorming van microthrombi in de vaten veroorzaakt door de ontstekingsreactie en de daaropvolgende rekrutering van immuuncellen en trombocyten staat bekend als immunotrombose. Dit draagt bij aan microvasculaire disfunctie en is een kenmerk van orgaanschade bij sepsis. (Greco et al., 2017)
Capillairen, arteriolen, venen en microlymfevaten maken allemaal deel uit van het microvasculair netwerk. Bij sepsis, zelfs wanneer de orgaanperfusie behouden blijft, zijn er vlekkerige gebieden van verminderde zuurstoftoevoer en -afvoer en functioneel shunting aangetoond. (Greco et al., 2017)
Leukocyten en trombocytenrecrutering, intravasculaire stolling, endotheel schade, verlies van surfactant, oxidatieve stress zijn allemaal mechanismen die mede ernstige longschade verzaken bij sepsis. Post mortem biopsies van patiënten die stierven met ARDS hebben een overmaat aan trombocyten en neutrofielen aangetoond in de pulmonale bloedvaten. De literatuur beschrijft verschillende rollen voor trombocyten in de pathogenese van ARDS. Er werd aangetoond dat uitputting van de trombocyten correleert met een verminderde rekrutering van neutrofielen en dat een verhoogde hoeveelheid trombocyten correleert met een verhoogde neutrofiele activering. (Greco et al., 2017)