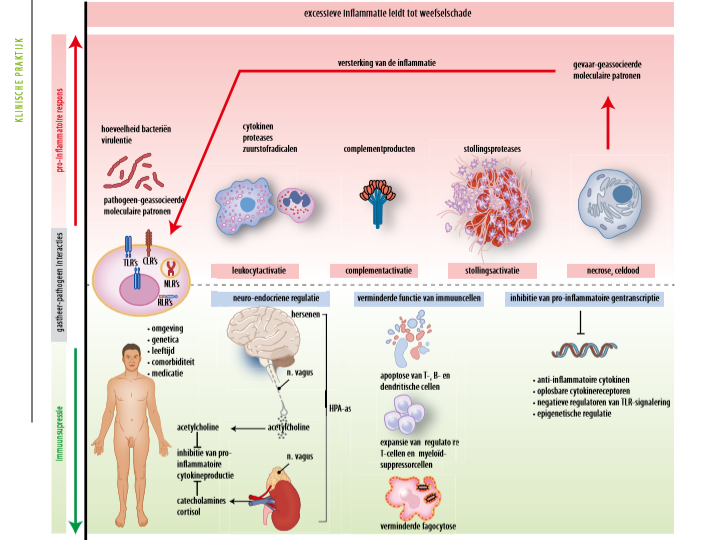
De pathogenese van sepsis is complex en omvat meerdere aspecten van de interactie tussen de infecterende micro-organismen en de gastheerreactie (Salomao et al., 2019). Het is een complex proces dat tot op heden nog steeds niet volledig wordt begrepen. Kenmerkend is dat het immuunsysteem het pathogeen en/of de uitgelokte immuunrespons niet onder controle krijgt waardoor er hyperinflammatie ontstaat. (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017) Deze systemische activering van het aangeboren immuunsysteem wordt overdreven geactiveerd en beschadigd het eigen lichaam. Het is dus de verdediging van de gastheer en niet de micro-organismen die het meest verantwoordelijk zijn voor de morbiditeit en mortaliteit van sepsis. (Yuki & Murakami, 2015) Dit wil zeggen dat niet enkel de initiële pro-inflammatoire pathways geactiveerd worden maar ook de anti-inflammatoire pathways (immuunsuppressie), welke later in de loop van sepsis de corrigerende respons kan verlagen (Evans, 2018).
Sepsis bestaat dus in feite uit twee fasen: een pro-inflammatoire reactie en een immuunsuppressieve (anti-inflammatoire) reactie (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017). De eerste fase begint met het herkennen van schadelijke micro-organismen en virulentiefactoren (pathogeengeassocieerde moleculaire patronen; (PAMP’s) alsook beschadigd weefsel (gevaar-geassocieerde moleculaire patronen; (DAMP’s) door immuuncellen zoals neutrofiele granulocyten, macrofagen en monocyten (Evans, 2018; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017; Yuki & Murakami, 2015). De patroonherkenningsreceptor (PRR) herkent deze PAMP's en DAMP's, en stimuleert de intracellulaire signalering die leidt tot de productie van ontstekingscytokines (Yuki & Murakami, 2015).
Van zodra deze pathogenen herkend zijn, worden er meerdere signaalcascades getriggered. Dit leidt dan weer tot de manifestatie van genen die coderen voor verschillende inflammatoire chemokines en cytokines. Deze defensiemechanismen beschermen de gastheer tegen pathogenen maar tegelijkertijd kan dit systeem ook schade toebrengen aan deze gastheer. Dit gebeurt door overmatige activatie van de PRR’s, welke bijdragen aan een schadelijke systemische inflammatie, complementactivatie, intravasculaire stollingsactivatie, weefselschade, vasodilatatie en multi-orgaanfalen. (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
Als de gastheer deze eerste fase overleeft, zijn er vaak kenmerken van immuunsuppressie, een chronische onderdrukking van zowel het aangeboren als het adaptieve immuunsysteem. Deze tweede fase van sepsis wordt gekenmerkt door neuro-endocriene dysregulatie, het vrijkomen van anti-inflammatoire cytokines en verminderd functioneren van de cellen van het afweersysteem. Een diepgaande leukocyten-apoptose en verminderde fagocytose zijn mede verantwoordelijk voor deze immuunsuppressie. De disfunctie van de endotheliale barrière treedt vroeg op in sepsis en septische shock in het bijzonder, wat leidt tot hypotensie en oedeem. (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
Sepsis bestaat dus in feite uit twee fasen: een pro-inflammatoire reactie en een immuunsuppressieve (anti-inflammatoire) reactie (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017). De eerste fase begint met het herkennen van schadelijke micro-organismen en virulentiefactoren (pathogeengeassocieerde moleculaire patronen; (PAMP’s) alsook beschadigd weefsel (gevaar-geassocieerde moleculaire patronen; (DAMP’s) door immuuncellen zoals neutrofiele granulocyten, macrofagen en monocyten (Evans, 2018; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017; Yuki & Murakami, 2015). De patroonherkenningsreceptor (PRR) herkent deze PAMP's en DAMP's, en stimuleert de intracellulaire signalering die leidt tot de productie van ontstekingscytokines (Yuki & Murakami, 2015).
Van zodra deze pathogenen herkend zijn, worden er meerdere signaalcascades getriggered. Dit leidt dan weer tot de manifestatie van genen die coderen voor verschillende inflammatoire chemokines en cytokines. Deze defensiemechanismen beschermen de gastheer tegen pathogenen maar tegelijkertijd kan dit systeem ook schade toebrengen aan deze gastheer. Dit gebeurt door overmatige activatie van de PRR’s, welke bijdragen aan een schadelijke systemische inflammatie, complementactivatie, intravasculaire stollingsactivatie, weefselschade, vasodilatatie en multi-orgaanfalen. (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
Als de gastheer deze eerste fase overleeft, zijn er vaak kenmerken van immuunsuppressie, een chronische onderdrukking van zowel het aangeboren als het adaptieve immuunsysteem. Deze tweede fase van sepsis wordt gekenmerkt door neuro-endocriene dysregulatie, het vrijkomen van anti-inflammatoire cytokines en verminderd functioneren van de cellen van het afweersysteem. Een diepgaande leukocyten-apoptose en verminderde fagocytose zijn mede verantwoordelijk voor deze immuunsuppressie. De disfunctie van de endotheliale barrière treedt vroeg op in sepsis en septische shock in het bijzonder, wat leidt tot hypotensie en oedeem. (Marshall, 2016; Wiersinga, van Zanten, Kaasjager, & van der Poll, 2017)
In een poging om deze complexe pathofysiologie te vereenvoudigen, kunnen vier hoofdkenmerken worden benadrukt: de vier ruiters van de septische apocalyps (Evans, 2018).
Endotheeldisfunctie
Gegeneraliseerde endotheliale activering verhoogt de adhesie (aantrekkingskracht) van leukocyten, met als gevolg een verhoogde leukocytentransmigratie naar de weefsels en een verhoogde permeabiliteit van het endotheel. In de longen kan dit leiden tot interstitieel longoedeem en in de darmen zorgt dit voor een toename van de bacteriële translocatie. Hierdoor worden de ontstekingscascades die al door microbiële producten zijn geïnitieerd mogelijks verergerd. (Evans, 2018)
Coagulopathie
Veranderde coagulatie komt zeer vaak voor bij sepsis. Door de beschadiging van het endotheel wordt de beschermende functie van het natuurlijke antistollingseiwit C-route verwijdert waardoor het endotheel wordt omgezet in een protrombotisch oppervlak. Bovendien activeren bacteriële micro-organismen en inflammatoire cytokines de weefseltromboplastine. Dit is de belangrijkste initiator van de extrinsieke route van bloedstolling. Deze protrombotische fase kan leiden tot verstopping van het microvasculair netwerk en tot gedissemineerde intravasculaire coagulatie. Grampositieve producten kunnen ook direct het contactstollingssysteem activeren. (Evans, 2018)
Cellulaire disfunctie
Ondanks dat er bij de ergste vorm van sepsis (met de dood als gevolg) een uitgesproken ernstige orgaandisfunctie aanwezig is, komen uit autopsies weinig bewijs van celdood naar voren komt. De moleculaire basis hiervan is nog steeds niet duidelijk maar een generaliseerde reductie in energieverbruik door de cellen suggereert een soort van winterslaap. Gelijktijdig met deze veranderingen in cellulaire functie zijn tal van metabole veranderingen, met name verhoogd katabolisme, insulineresistentie en hyperglycemie. (Evans, 2018)
Cardiovasculaire disfunctie
Patiënten met sepsis hebben een verminderde systemische vaatweerstand (SVR) maar wel een normale of verhoogde cardiale output, ook wel bekend als de hyperdynamische circulatie. De cardiale output blijft behouden maar gaat ten koste van de linkerventrikel, deze dilateert waardoor het linkerventrikel eind-diastolisch volume toeneemt en de ejectiefractie en slagvolume vermindert. Vervolgens kan dit leiden tot hypotensie, toch wel kenmerkend voor septische shock. Wijzigingen in de SVR worden waarschijnlijk grotendeels veroorzaakt door een overmatige productie van de vasodilatator stikstofmonoxide in het vasculatuur, wat moeilijk te corrigeren is met vasopressoren. Slechte weefselperfusie ligt waarschijnlijk ook ten grondslag aan het verhoogde lactaat dat wordt gezien bij septische shock, hoewel andere mechanismen mogelijk zijn. (Evans, 2018)
Endotheeldisfunctie
Gegeneraliseerde endotheliale activering verhoogt de adhesie (aantrekkingskracht) van leukocyten, met als gevolg een verhoogde leukocytentransmigratie naar de weefsels en een verhoogde permeabiliteit van het endotheel. In de longen kan dit leiden tot interstitieel longoedeem en in de darmen zorgt dit voor een toename van de bacteriële translocatie. Hierdoor worden de ontstekingscascades die al door microbiële producten zijn geïnitieerd mogelijks verergerd. (Evans, 2018)
Coagulopathie
Veranderde coagulatie komt zeer vaak voor bij sepsis. Door de beschadiging van het endotheel wordt de beschermende functie van het natuurlijke antistollingseiwit C-route verwijdert waardoor het endotheel wordt omgezet in een protrombotisch oppervlak. Bovendien activeren bacteriële micro-organismen en inflammatoire cytokines de weefseltromboplastine. Dit is de belangrijkste initiator van de extrinsieke route van bloedstolling. Deze protrombotische fase kan leiden tot verstopping van het microvasculair netwerk en tot gedissemineerde intravasculaire coagulatie. Grampositieve producten kunnen ook direct het contactstollingssysteem activeren. (Evans, 2018)
Cellulaire disfunctie
Ondanks dat er bij de ergste vorm van sepsis (met de dood als gevolg) een uitgesproken ernstige orgaandisfunctie aanwezig is, komen uit autopsies weinig bewijs van celdood naar voren komt. De moleculaire basis hiervan is nog steeds niet duidelijk maar een generaliseerde reductie in energieverbruik door de cellen suggereert een soort van winterslaap. Gelijktijdig met deze veranderingen in cellulaire functie zijn tal van metabole veranderingen, met name verhoogd katabolisme, insulineresistentie en hyperglycemie. (Evans, 2018)
Cardiovasculaire disfunctie
Patiënten met sepsis hebben een verminderde systemische vaatweerstand (SVR) maar wel een normale of verhoogde cardiale output, ook wel bekend als de hyperdynamische circulatie. De cardiale output blijft behouden maar gaat ten koste van de linkerventrikel, deze dilateert waardoor het linkerventrikel eind-diastolisch volume toeneemt en de ejectiefractie en slagvolume vermindert. Vervolgens kan dit leiden tot hypotensie, toch wel kenmerkend voor septische shock. Wijzigingen in de SVR worden waarschijnlijk grotendeels veroorzaakt door een overmatige productie van de vasodilatator stikstofmonoxide in het vasculatuur, wat moeilijk te corrigeren is met vasopressoren. Slechte weefselperfusie ligt waarschijnlijk ook ten grondslag aan het verhoogde lactaat dat wordt gezien bij septische shock, hoewel andere mechanismen mogelijk zijn. (Evans, 2018)